题目内容
17.已知反应:2NO2+2NaOH═NaNO3+NaNO2+H2O;NO+NO2+2NaOH═2NaNO2+H2O现有XmolNO2和YmolNO(X>Y)组成的混合气体,欲用m L含nmolNaOH的溶液吸收,使该混合气体全部转化成盐(NaNO3和NaNO2)进入溶液,则n的值至少是( )
| A. | X/m mol | B. | 2X/3mol | C. | (X+Y)mol | D. | 2(X+Y)/3mol |
分析 根据组成守恒,NaNO3和NaNO2中钠与氮之比为1:1,所以n(NaOH)=n(NO2)+n(NO)=(X+Y)mol,由此分析解答.
解答 解:现有XmolNO2和YmolNO(X>Y)组成的混合气体,欲用m L含nmolNaOH的溶液吸收,恰好完全反应,生成,NaNO3和NaNO2,根据组成守恒,NaNO3和NaNO2中钠与氮之比为1:1,所以n(NaOH)=n(NO2)+n(NO)=(X+Y)mol,故选C.
点评 本题考查混合物计算、根据方程式计算,原子守恒是关键,属于字母型计算,增大计算难度,为易错题目,难度中等.

练习册系列答案
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案
相关题目
5.25℃,两种酸的电离常数如下表.
下列叙述中正确的是( )
| Ka1 | Ka2 | |
| H2A | 1.3×10-2 | 6.3×10-6 |
| H2B | 4.2×10-7 | 5.6×10-7 |
| A. | H2A的电离方程式:H2A═2H++A2- | |
| B. | 常温下,在水中Na2B的水解平衡常数为:Ka1=$\frac{K_W}{{4.2×{{10}^{-7}}}}$ | |
| C. | 等浓度的Na2A和Na2B溶液,由水电离产生的H+浓度大小关系为:前者大于后者 | |
| D. | 向Na2B溶液中加入少量H2A溶液,可发生反应:B2-+H2A=A2-+H2B |
12.下列相关反应的离子方程式书写正确的是( )
| A. | 氢氧化铁溶于氢碘酸:Fe(OH)3+3H+═Fe3++3H2O | |
| B. | Al片与少量NaOH溶液反应,产生气体:2Al+2OH-+2H2O═2Al(OH)3+3H2↑ | |
| C. | 向碳酸氢铵溶液中加过量石灰水并加热:NH4++OH-═NH3•H2O | |
| D. | 用酸化的高锰酸钾溶液氧化双氧水:2MnO4-+6H++5H2O═2Mn2++5O2↑+8H2O |
9.下列叙述中,正确的是( )
①电解池是将化学能转变成电能的装置,原电池是将电能转变成化学能的装置
②需要通电后才可以发生或进行的有:电离、电泳、电解、电镀、电化学腐蚀
③金属和石墨导电均为物理变化,电解质溶液导电是化学变化
④不能自发进行的氧化还原反应,通过电解的原理有可能实现
⑤电镀过程相当于金属的“迁移”,可视为物理变化.
①电解池是将化学能转变成电能的装置,原电池是将电能转变成化学能的装置
②需要通电后才可以发生或进行的有:电离、电泳、电解、电镀、电化学腐蚀
③金属和石墨导电均为物理变化,电解质溶液导电是化学变化
④不能自发进行的氧化还原反应,通过电解的原理有可能实现
⑤电镀过程相当于金属的“迁移”,可视为物理变化.
| A. | ①②③④ | B. | ③④⑤ | C. | ③④ | D. | ④ |
6.向1L0.1mol/L的Na2SO3溶液中滴加盐酸(假设反应前后溶液体积不变),溶液中水电离出的OH-离子浓度随盐酸的用量关系如图所示.图中各点溶液pH随n(SO32-):n(HSO3-)变化关系如表,下列叙述不正确的是( ) 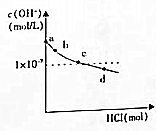

| 坐标对应点 | a | b | c | d |
| n(SO32-)n:(HSO3-) | 91:9 | 1:1 | 9:91 | |
| pH | >8.2 | 8.2 | 7.2 | 6.2 |
| A. | b点溶液中:水电离出的c(OH-)=1×10-5.8mol/L | |
| B. | c点溶液中:c(Na+)>c(SO32-)>c(HSO3-)>c(OH-)>c(H+) | |
| C. | d点溶液中HSO3-的电离大于水解 | |
| D. | d点溶液中:c(Na+)<c(SO32-)+c(HSO3-)+c(Cl-) |
16.下列化学方程式不能用离子方程式2H++CO32-=H2O+CO2↑表示的是( )
| A. | 2HCl+Na2CO3═2NaCl+H2O+CO2↑ | B. | 2HNO3+BaCO3═Ba(NO3)2+H2O+CO2↑ | ||
| C. | H2SO4+Na2CO3═Na2SO4+H2O+CO2↑ | D. | H2SO4+(NH4)2CO3═(NH4)2SO4+H2O+CO2↑ |
 (或
(或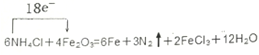 );
);