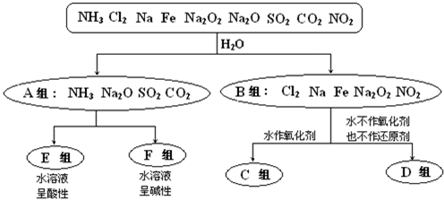
题目内容
18.下列说法正确的是( )| A. | 化学键的断裂和形成是化学反应能量变化的主要原因 | |
| B. | 伴有能量变化的物质变化都是化学变化 | |
| C. | 在一个确定的化学反应中,反应物的总能量与生成物的总能量一定不同 | |
| D. | 在一个确定的化学反应中,反应物的总能量总是高于生成物的总能量 |
分析 A.化学反应的实质为化学键的断裂和形成,断裂吸收能量,形成释放能量;
B.物理变化中也有能量变化;
C、根据化学反应中,反应物的总能量与生成物的总能量一定不同;
D、根据化学反应中,反应物的总能量高于生成物的总能量时,反应放热,反应物的总能量低于生成物的总能量时,反应吸热.
解答 解:A.化学反应的实质为化学键的断裂和形成,断裂吸收能量,形成释放能量,则化学键的断裂和形成是化学反应能量变化的主要原因,故A正确;
B.物理变化中也有能量变化,如浓硫酸稀释,物质三态变化等,不发生化学变化,故B错误;
C、因化学反应中,反应物的总能量与生成物的总能量一定不同,不是放热,就是吸热,故C正确;
D、根据化学反应中,反应物的总能量高于生成物的总能量时,反应放热,反应物的总能量低于生成物的总能量时,反应吸热,故D错误;
故选AC.
点评 本题主要考查了化学反应中能量变化的原因,难度不大,根据课本知识即可完成.

练习册系列答案
相关题目
6.如图是元素周期表的轮廓图,通常用于制造农药的元素所在的区域是( )
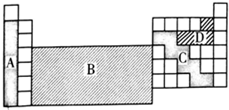

| A. | A | B. | B | C. | C | D. | D |
13.在一定条件下MO3-与M-发生反应;MO3-+5M-+6H+═3M2+3H2O,则下列关于M元素的叙述中正确的是( )
| A. | M的氢化物的水溶液呈酸性 | B. | M2在常温常压下一定是气体 | ||
| C. | MO3-中的M元素只能被还原 | D. | M位于元素周期表的第VA族 |
6.工业生产钠和烧碱的原理如下:①电解熔融氯化钠制钠:2NaCl(熔融)$\frac{\underline{\;电解\;}}{\;}$2Na+Cl2↑
②电解饱和食盐水制烧碱:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2 ↑
下列有关说法正确的是 ( )
②电解饱和食盐水制烧碱:2NaCl+2H2O$\frac{\underline{\;电解\;}}{\;}$2NaOH+H2↑+Cl2 ↑
下列有关说法正确的是 ( )
| A. | 在反应①和②中,氯化钠均既是氧化剂,又是还原剂 | |
| B. | 在反应①中氯气是还原产物,在反应②中氢气是还原产物 | |
| C. | 若标准状况下生成等体积的气体,则反应①和②中转移电子总数相等 | |
| D. | 若消耗等质量的氯化钠,则反应①和②中转移电子总数相等 |
7.如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法正确的是( )


| A. | 该硫酸的物质的量浓度为9.2mol/L | |
| B. | 配制500mL 4.6mol/L的稀硫酸需取该硫酸125mL | |
| C. | 1mol Cu与足量的该硫酸反应产生2g氢气 | |
| D. | 等质量的水与该硫酸混合所得溶液的物质的量浓度大于9.2mol/L |

 .
. .
.