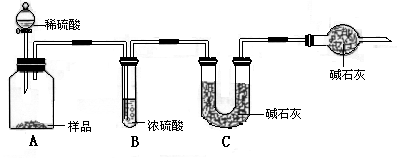
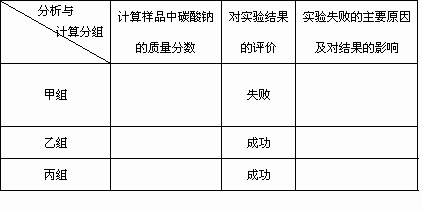
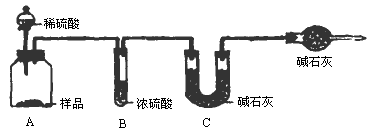
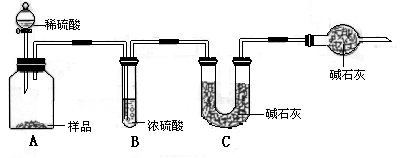
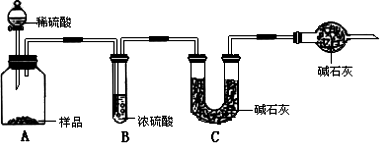
题目内容
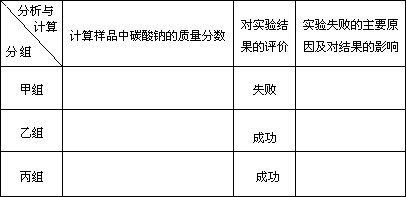
| |||||||||||
解析:
(1) |
碳酸氢钠时从含有大量NH4+、Na+、Cl-、HCO3-的饱和溶液中析出的,所以碳酸氢钠晶体中混有氯化钠杂质,又由于氯化钠受热不分解,导致工业纯碱中含有少量的氯化钠 |
(2) |
|

下图是某工厂对海水资源进行综合利用的示意图.
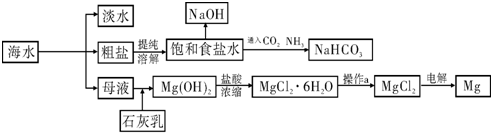
请回答下列问题:
(1)请列举一种海水淡化的方法
(2)工业上常用离子交换膜电解槽生产NaOH,电解过程中大量通过离子交换膜的离子是
(3)侯氏制碱法中首先向饱和食盐水中通入CO2和NH3制得NaHCO3,先通入
(填化学式),理由是
(4)镁是一种用途很广泛的金属材料,目前世界上60%的镁从海水中提取.已知有关物质的熔沸点数据如下:
| MgO | MgCl2 | |
| 熔点/℃ | 2852 | 714 |
| 沸点/℃ | 3600 | 1412 |
| |||||||||||