题目内容
下列物质的量浓度关系不正确的是( )
| A、常温下0.1 mol/L的下列溶液①NH4Al(SO4)2 ②NH3?H2O③NH4Cl ④CH3COONH4中,c(NH4+)由大到小的顺序是:①>③>④>② |
| B、将0.1 mol?L-1的NaHS和0.1 mol?L-1Na2S溶液等体积混合:c(S2-)+2c(OH-)=2c(H+)+c(HS-)+3c(H2S) |
| C、将0.2 mol CH3COONa晶体和0.1 mol HCl气体同时溶解于同一烧杯的水中,制得1 L溶液:c(CH3COO-)+c(OH-)=0.10 mol?L-1 |
| D、已知HClO+Na2CO3=NaClO+NaHCO3,在等物质的量浓度等体积次氯酸溶液与碳酸钠溶液混合溶液中:c(HClO)+c(H+)+c(H2CO3)═c(OH-)+c(CO32-) |
考点:离子浓度大小的比较
专题:
分析:A、①铝离子水解抑制铵根离子的水解;②弱碱电离,且电离的程度很弱;③铵根离子水解;④醋酸根离子水解促进铵根离子水解;
B、根据0.1mol?L-1的NaHS和0.1mol?L-1 Na2S混合溶液中物料守恒和电荷守恒进行判断;
C、根据物料守恒得c(CH3COOH)+c(CH3COO-)=0.20mol?L-1;
D、在等物质的量浓度等体积次氯酸溶液与碳酸钠溶液混合溶液中存在溶质NaHCO3和NaClO.
B、根据0.1mol?L-1的NaHS和0.1mol?L-1 Na2S混合溶液中物料守恒和电荷守恒进行判断;
C、根据物料守恒得c(CH3COOH)+c(CH3COO-)=0.20mol?L-1;
D、在等物质的量浓度等体积次氯酸溶液与碳酸钠溶液混合溶液中存在溶质NaHCO3和NaClO.
解答:
解:A、同浓度的下列溶液:①NH4Al(SO4)2②NH3?H2O③NH4Cl,④CH3COONH4,因①中铝离子水解抑制铵根离子的水解;②弱碱电离,且电离的程度很弱;③中铵根离子水解;④醋酸根离子水解促进铵根离子水解,则c(NH4+)由大到小的顺序是:①>③>④>②,故A正确;
B、将0.1mol?L-1的NaHS和0.1mol?L-1 Na2S溶液等体积混合,根据物料守恒可得:2c(Na+)=3[c(HS-)+c(H2S)+c(S2-)],根据电荷守恒可知:c(H+)+c(Na+)=2c(S2-)+c(OH-)+c(HS-),由电荷守恒和物料守恒联立可得:c(S2-)+2c(OH-)=2c(H+)+c(HS-)+3c(H2S),故B正确;
C、将0.2 mol CH3COONa晶体和0.1 mol HCl气体同时溶解于同一烧杯的水中,制得1 L溶液,溶液中存在物料守恒:c(CH3COO-)+c(OH-)=0.20 mol/L,故C错误;
D、在等物质的量浓度等体积次氯酸溶液与碳酸钠溶液混合溶液中存在溶质NaHCO3和NaClO;根据物料守恒得c(Na+)═c(HClO)+c(ClO-)+c(HCO3-)+c(H2CO3)+c(CO32-),电荷守恒得c(Na+)+c(H+)═c(ClO-)+c(HCO3-)+2c(CO32-)+c(OH-),得到:c(HClO)+c(H+)+c(H2CO3)═c(OH-)+c(CO32-),故D正确;
故选C.
B、将0.1mol?L-1的NaHS和0.1mol?L-1 Na2S溶液等体积混合,根据物料守恒可得:2c(Na+)=3[c(HS-)+c(H2S)+c(S2-)],根据电荷守恒可知:c(H+)+c(Na+)=2c(S2-)+c(OH-)+c(HS-),由电荷守恒和物料守恒联立可得:c(S2-)+2c(OH-)=2c(H+)+c(HS-)+3c(H2S),故B正确;
C、将0.2 mol CH3COONa晶体和0.1 mol HCl气体同时溶解于同一烧杯的水中,制得1 L溶液,溶液中存在物料守恒:c(CH3COO-)+c(OH-)=0.20 mol/L,故C错误;
D、在等物质的量浓度等体积次氯酸溶液与碳酸钠溶液混合溶液中存在溶质NaHCO3和NaClO;根据物料守恒得c(Na+)═c(HClO)+c(ClO-)+c(HCO3-)+c(H2CO3)+c(CO32-),电荷守恒得c(Na+)+c(H+)═c(ClO-)+c(HCO3-)+2c(CO32-)+c(OH-),得到:c(HClO)+c(H+)+c(H2CO3)═c(OH-)+c(CO32-),故D正确;
故选C.
点评:本题考查了电解质溶液中电荷守恒和物料守恒,离子浓度大小比较,掌握基础是解题关键,题目难度中等.

练习册系列答案
 全能测控期末小状元系列答案
全能测控期末小状元系列答案
相关题目
关于下列各装置图的叙述中,正确的是( )
A、 验证化学能转化为电能 |
B、 比较硫、碳、硅三种元素的非金属行强弱 |
C、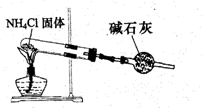 实验室制取NH3 |
D、 分离沸点不同且互溶的液体混合物 |
将一定量的醋酸与一定量的NaOH溶液混合,下列说法中不正确的是( )
| A、若混合后呈中性,测混合后的溶液中一定存在:c(Na+)=c(CH3COO-)>c(OH-)=c(H+) |
| B、若混合后呈酸性,则混合后的溶液中可能存在:c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+)>c(OH-) |
| C、若混合后呈碱性,则混合后的溶液中可能存在:c(Na+)>c(OH-)>c(CH3COO-)>c(CH3COOH) |
| D、若混合后的溶液中存在c(CH3COO-)+c(CH3COOH)=2c(Na+),则也一定存在c(OH-)+c(CH3COO-)=c(CH3COOH)+c(H+)等式 |
根据VSEPR模型判断下列各组分子或离子结构相同的是( )
| A、SO2和CO2 |
| B、BF3和NH3 |
| C、NH3和H2O |
| D、CH4和NH4+ |
下列叙述正确的是( )
| A、常温下,10 mL 0.02 mol?L-1 HCl溶液与10 mL 0.02 mol?L-1 Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12 |
| B、常温下,向AgCl的饱和溶液中加入NaCl固体,有固体析出,且AgCl的Ksp变小 |
| C、在0.1 mol?L-1 CH3COONa溶液中,c(OH-)>c(CH3COOH)+c(H+) |
| D、常温下pH=4的NaHC2O4溶液中:c(H2C2O4)>c(C2O42-) |
 SO2通入BaCl2溶液中并不产生沉淀,而通入另一种气体后可以产生白色沉淀.则图中右侧Y形管中放置的药品组合不符合要求的是(必要时可以加热)( )
SO2通入BaCl2溶液中并不产生沉淀,而通入另一种气体后可以产生白色沉淀.则图中右侧Y形管中放置的药品组合不符合要求的是(必要时可以加热)( )| A、Cu和浓硝酸 |
| B、大理石和稀盐酸 |
| C、CaO和浓氨水 |
| D、高锰酸钾溶液和浓盐酸 |
下列有关化学用语表示正确的是( )
A、NH4Br的电子式: | ||
B、S原子的结构示意图: | ||
| C、乙醇的结构简式:C2H6O | ||
D、原子核内有18个中子的氯原子:
|
 某小组以CoCl2?6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X.为确定其组成,进行如下实验.
某小组以CoCl2?6H2O、NH4Cl、H2O2、浓氨水为原料,在活性炭催化下,合成了橙黄色晶体X.为确定其组成,进行如下实验.