题目内容
10.100g CaCO3与30g SiO2的混合物加强热,使之充分反应.请计算得到气体的体积为多少(标准状况)?分析 发生CaCO3+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑、CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,n(CaCO3)=$\frac{100g}{100g/mol}$=1mol,n(SiO2)=$\frac{30g}{60g/mol}$=0.5mol,由反应可知n(CO2)=n(CaCO3),结合V=nVm计算.
解答 解:发生CaCO3+SiO2$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑、CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑,
反应可知n(CO2)=n(CaCO3),
n(CaCO3)=$\frac{100g}{100g/mol}$=1mol,则气体的体积为1mol×22.4L/mol=22.4L,
答:反应生成气体体积为22.4 L.
点评 本题考查化学反应方程式的计算,为高频考点,把握发生的反应为解答的关键,侧重分析与计算能力的考查,注意气体的物质的量等于碳酸钙的物质的量,题目难度不大.

练习册系列答案
 智慧小复习系列答案
智慧小复习系列答案
相关题目
19.下列说法不正确的是( )
| A. | 聚乙烯、天然橡胶都是由高分子化合物组成的物质 | |
| B. | 用高锰酸钾溶液不可以鉴别直馏汽油和裂化汽油 | |
| C. | 有机物均含有C元素,但不是所有有机物均能发生燃烧反应 | |
| D. | 煤的气化、液化、干馏都属于化学变化 |
20.把0.05molNaOH晶体分别加入到下列100mL液体中,溶液导电性变化最小的是( )
| A. | 自来水 | B. | 0.5 mol/L盐酸 | C. | 0.5mol/L 氨水 | D. | 0.5 mol/LNaNO3 |
5.某饱和一元醇的分子式为C5H12O,在一定条件下可以被催化氧化得到醛,则该饱和一元醇的结构简式最多有( )
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
15.硫酸亚铁铵晶体[(NH4)2Fe(SO4)2•6H2O]是一种稳定的还原剂,其制备流程如图1:
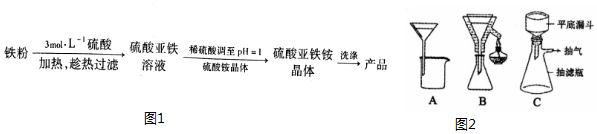
(1)硫酸浓度过大,反应过快同时会使FeSO4溶液中混有Fe3+(填离子符号).
(2)铁粉中混有少量P、S等元素,反应过程中产生的气体有刺激性气味,实验中应采取的措施在通风橱里进行.
(3)铁粉未完全反应,就得趁热过滤,图2中合适的过滤装置是B.
几种物质的溶解度(g/100gH2O)
(4)利用FeSO4与(NH4)2SO4制备(NH4)2Fe(SO4)2•6H2O的原理是由于(NH4)2Fe(SO4)2•6H2O溶解度较小,发生FeSO4+(NH4)2SO4+6H2O=(NH4)2Fe(SO4)2•6H2O,析出晶体(用化学方程式及必要的文字说明).
(5)将(NH4)2SO4晶体加入到FeSO4滤液中,加热搅拌至全部溶解,再蒸发浓缩至溶液表面有晶膜出现时,静置冷却结晶,抽滤,用少量乙醇洗涤晶体2~3次,将晶体放在表面皿上晾干,最终得到的产品质量为19.6g,本次实验产率为77.8%(本次实验使用4.0g铁粉,剩余0.4g未反应).

(1)硫酸浓度过大,反应过快同时会使FeSO4溶液中混有Fe3+(填离子符号).
(2)铁粉中混有少量P、S等元素,反应过程中产生的气体有刺激性气味,实验中应采取的措施在通风橱里进行.
(3)铁粉未完全反应,就得趁热过滤,图2中合适的过滤装置是B.
几种物质的溶解度(g/100gH2O)
| 物质 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 70℃ |
| FeSO4•7H2O | 28.8 | 40.0 | 48.0 | 60.0 | 73.3 | - | - |
| (NH4)2SO4 | 70.6 | 73 | 75.4 | 78.0 | 81 | 84.5 | 94.9 |
| (NH4)2SO4•FeSO4•6H2O | 14.5 | 18.1 | 21.2 | 24.5 | 27.9 | 31.3 | 38.5 |
(5)将(NH4)2SO4晶体加入到FeSO4滤液中,加热搅拌至全部溶解,再蒸发浓缩至溶液表面有晶膜出现时,静置冷却结晶,抽滤,用少量乙醇洗涤晶体2~3次,将晶体放在表面皿上晾干,最终得到的产品质量为19.6g,本次实验产率为77.8%(本次实验使用4.0g铁粉,剩余0.4g未反应).
2.下列说法中正确的是( )
| A. | 不慎将酸或碱液溅入眼内,立即闭上眼睛,用手揉擦 | |
| B. | 实验桌上的酒精灯倾倒了燃烧起来,马上用湿布扑灭 | |
| C. | 皮肤上溅有较多的浓硫酸,赶紧用水冲洗 | |
| D. | 衣服沾上大量的浓氢氧化钠溶液,需将此衣服浸泡在盛水的盆中 |
19.同温同压下,含有相同氧原子数的SO2与CO气体,下列叙述正确的是( )
| A. | 物质的量之比为2:1 | B. | 体积之比为1:2 | ||
| C. | 质量之比为16:7 | D. | 密度之比为7:16 |
20.某有机物的结构简式如图所示,下列说法错误的是( )
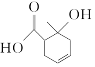

| A. | 与乙酸互为同系物 | |
| B. | 含有两种含氧官能团 | |
| C. | 可使Br2的CCl4溶液褪色 | |
| D. | 既可以发生取代反应又可以发生加成反应 |