��Ŀ����
���ܵ������ˮ��Һ�д����ŵ���ƽ�⡣�ڳ����£���Һ��������ӵ�Ũ�������ǻ�ѧ������Ϊ���εij˻���һ�����������ܶȻ�����(Ksp)�����磺Cu(OH)2 Cu2+��2OH-��Ksp��c(Cu2+)��[c(OH-)]2��
Cu2+��2OH-��Ksp��c(Cu2+)��[c(OH-)]2��
2��10-20������Һ�и������ӵ�Ũ�ȷ��εij˻������ܶȻ�ʱ���������������֮�����ܽ⡣
��1��ijCuSO4��Һ��c(Cu2+)��0.02 mol/L����Ҫ����Cu(OH)2������Ӧ������Һ��pH��ʹ֮����__________________��
��2��Ҫʹ0.2 mol��L-1 CuSO4��Һ��Cu2+������Ϊ��ȫ(ʹCu2+Ũ�Ƚ���ԭ����ǧ��֮һ)����Ӧ����Һ�����NaOH��Һ��ʹ��Һ��pHΪ__________________��
 Cu2+��2OH-��Ksp��c(Cu2+)��[c(OH-)]2��
Cu2+��2OH-��Ksp��c(Cu2+)��[c(OH-)]2��2��10-20������Һ�и������ӵ�Ũ�ȷ��εij˻������ܶȻ�ʱ���������������֮�����ܽ⡣
��1��ijCuSO4��Һ��c(Cu2+)��0.02 mol/L����Ҫ����Cu(OH)2������Ӧ������Һ��pH��ʹ֮����__________________��
��2��Ҫʹ0.2 mol��L-1 CuSO4��Һ��Cu2+������Ϊ��ȫ(ʹCu2+Ũ�Ƚ���ԭ����ǧ��֮һ)����Ӧ����Һ�����NaOH��Һ��ʹ��Һ��pHΪ__________________��
��1��5
��2��6
��2��6

��ϰ��ϵ�д�
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
�����Ŀ
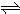 Cu2++2OH-��Ksp=c��Cu2+��?[c��OH-��]2=2��10-20������Һ�и�����Ũ�ȷ��εij˻������ܶȻ�ʱ���������������֮�����ܽ⣮
Cu2++2OH-��Ksp=c��Cu2+��?[c��OH-��]2=2��10-20������Һ�и�����Ũ�ȷ��εij˻������ܶȻ�ʱ���������������֮�����ܽ⣮