题目内容
| 时间(s) n(mol) |
0 | 20 | 40 | 60 | 80 | 100 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
②计算在80℃时该反应的平衡常数K=
③反应进行至100s后将反应混合物的温度降低,混合气体的颜色(填“变浅”、“变深”或“不变”)
④要增大该反应的K值,可采取的措施有(填序号)
A.增大N2O4的起始浓度B.向混合气体中通入NO2 C.使用高效催化剂 D.升高温度
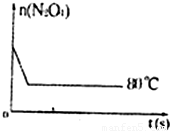
⑤如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线


(2)难溶电解质在水溶液中存在着电离平衡.在常温下,溶液里各离子浓度以它们化学计量数为方次的乘积是一个常数,叫溶度积常数(Ksp).例如Cu(OH)2(S)?Cu2+(aq)+2OH-(aq),Ksp=c(Cu2+)?[c(OH-)]2=2×10-20当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.若某CuSO4溶液里c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,应调整溶液pH,使之大于
要使0.2mol/L的CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使溶液pH值为
(3)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色.则该溶液呈
②由表格中的数据可知,平衡时,c(NO2)=
| 0.6mol |
| 1L |
③该反应为吸热反应,若降低温度,平衡逆向移动;
④增大该反应的平衡常数,可使平衡正向移动,以此分析;
⑤反应在60℃时达到平衡,反应速率减小,该反应为吸热反应,降低温度逆向移动,则N2O4物质的量变大;
(2)c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,根据Ksp计算pH;0.2mol/L的CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,c(Cu2+)=0.0002mol/L,根据Ksp计算pH;
(3)碳酸根离子水解显碱性,并借助水解平衡移动分析原因.
| 0.04mol/L |
| 20s |
②由表格中的数据可知,平衡时,c(NO2)=
| 0.6mol |
| 2L |
K=
| (0.3mol/L)2 |
| 0.05mol/L |
③该反应为吸热反应,若降低温度,平衡逆向移动,二氧化氮的浓度减小,颜色变浅,故答案为:变浅;
④增大该反应的平衡常数,可使平衡正向移动,AB均使K减小,C使K不变,该反应为吸热反应,D升高温度平衡正向移动,K增大,故答案为:D;
⑤反应在60℃时达到平衡,反应速率减小,该反应为吸热反应,降低温度逆向移动,则N2O4物质的量变大,如图
 ,
,故答案为:
 ;
;(2)Ksp=c(Cu2+)?[c(OH-)]2=2×10-20,c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,c(0H-)=
|
|
(3)纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色,是因碳酸根离子水解显碱性,NaOH与氯化钡不反应,而碳酸钠与氯化钡反应导致水解平衡逆向移动,氢氧根离子浓度减小,则向红色溶液中加入足量BaCl2溶液,如果溶液还显红色说明甲正确,红色褪去说明乙正确,
故答案为:碱;向红色溶液中加入足量BaCl2溶液,如果溶液还显红色说明甲正确,红色褪去说明乙正确.

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案(1)80℃时,将0.40 mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4 (g)  2NO2 (g) △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 (g) △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) n(mol) | 0 | 20 | 40 | 60 | 80 | 110 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
②计算20s—40s内用NO2表示的平均反应速率为 mol/(L·s)
③计算在80℃时该反应的平衡常数K= ;
(2)若(1)中反应进行至110s后,保持温度和体积不变,向容器中再加入0.2mol N2O4,此时,平衡朝_______方向移动;建立新平衡后,N2O4的转化率_______75%(填“>、<或=”);
(3)若(1)中反应进行至110s后,保持温度和体积不变,向容器中再加入0.2mol N2O4和0.1mol NO2时,v正________ v逆(填“>、<或=”)
(1)80℃时,将0.40 mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4
(g)  2NO2 (g) △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 (g) △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
|
时间(s) n(mol) |
0 |
20 |
40 |
60 |
80 |
110 |
|
n(N2O4) |
0.40 |
a |
0.20 |
c |
d |
e |
|
n(NO2) |
0.00 |
0.24 |
b |
0.52 |
0.60 |
0.60 |
①上表中c =___________;e =_____________
②计算20s—40s内用NO2表示的平均反应速率为 mol/(L·s)
③计算在80℃时该反应的平衡常数K= ;
(2)若(1)中反应进行至110s后,保持温度和体积不变,向容器中再加入0.2mol N2O4,此时,平衡朝_______方向移动;建立新平衡后,N2O4的转化率_______75%(填“>、<或=”);
(3)若(1)中反应进行至110s后,保持温度和体积不变,向容器中再加入0.2mol N2O4和0.1mol NO2时,v正________ v逆(填“>、<或=”)
(1)80℃时,将0.40 mol的N2O4气体充入2L已经抽空的固定容积的密闭容器中,发生如下反应:N2O4 (g) ![]() 2NO2 (g) △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
2NO2 (g) △H>0,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) n(mol) | 0 | 20 | 40 | 60 | 80 | 110 |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
①上表中c =___________;e =_____________
②计算20s—40s内用NO2表示的平均反应速率为 mol/(L·s)
③计算在80℃时该反应的平衡常数K= ;
(2)若(1)中反应进行至110s后,保持温度和体积不变,向容器中再加入0.2mol N2O4,此时,平衡朝_______方向移动;建立新平衡后,N2O4的转化率_______75%(填“>、<或=”);
(3)若(1)中反应进行至110s后,保持温度和体积不变,向容器中再加入0.2mol N2O4和0.1mol NO2时,v正________ v逆(填“>、<或=”)
| 时间(s) n(mol) | 20 | 40 | 60 | 80 | 100 | |
| n(N2O4) | 0.40 | a | 0.20 | c | d | e |
| n(NO2) | 0.00 | 0.24 | b | 0.52 | 0.60 | 0.60 |
②计算在80℃时该反应的平衡常数K=______;
③反应进行至100s后将反应混合物的温度降低,混合气体的颜色(填“变浅”、“变深”或“不变”)______;
④要增大该反应的K值,可采取的措施有(填序号)______
A.增大N2O4的起始浓度B.向混合气体中通入NO2 C.使用高效催化剂 D.升高温度
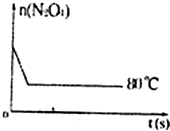
⑤如图是80℃时容器中N2O4物质的量的变化曲线,请在该图中补画出该反应在60℃时N2O4物质的量的变化曲线______.
(2)难溶电解质在水溶液中存在着电离平衡.在常温下,溶液里各离子浓度以它们化学计量数为方次的乘积是一个常数,叫溶度积常数(Ksp).例如Cu(OH)2(S)?Cu2+(aq)+2OH-(aq),Ksp=c(Cu2+)?[c(OH-)]2=2×10-20当溶液中各离子浓度方次的乘积大于溶度积时,则产生沉淀,反之固体溶解.若某CuSO4溶液里c(Cu2+)=0.02mol/L,如果生成Cu(OH)2沉淀,应调整溶液pH,使之大于______;
要使0.2mol/L的CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一)则应向溶液里加NaOH溶液,使溶液pH值为______.
(3)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色.则该溶液呈______性.在分析该溶液遇酚酞呈红色原因时,甲同学认为是配制溶液所用的纯碱样品中混有NaOH所致;乙同学认为是溶液中Na2CO3电离出的CO32-水解所致.请你设计一个简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论)
______.