题目内容
17. 在一密闭容器中有如下反应:L(s)+aG(g)?bR(g)温度和压强对该反应的影响如图所示,其中压强P1<P2,下列判断错误的是( )
在一密闭容器中有如下反应:L(s)+aG(g)?bR(g)温度和压强对该反应的影响如图所示,其中压强P1<P2,下列判断错误的是( )| A. | 正反应为吸热反应 | B. | 化学方程式中的计量数a>b | ||
| C. | G的转化率随温度升高而增大 | D. | 增大压强,容器内气体质量不变 |
分析 根据图象知,温度越高,G的体积分数越小,说明该反应的正反应是吸热反应,增大压强,G的体积分数减小,则该反应是一个反应前后气体体积减小的反应.
解答 解:A.根据图象知,温度越高,G的体积分数越小,说明该反应的正反应是吸热反应,故A正确;
B.增大压强,G的体积分数减小,则该反应是一个反应前后气体体积减小的反应,则a>b,故B正确;
C.温度越高,平衡向正反应方向移动,所以G的转化率随温度升高而增大,故C正确;
D.增大压强,平衡向正反应方向移动,所以容器内气体质量增大,故D错误;
故选D.
点评 本题考查了温度、压强对化学平衡的影响,明确温度、压强与化学平衡移动方向之间的关系是解本题关键,注意L是固体,为易错点.

练习册系列答案
 教材全解字词句篇系列答案
教材全解字词句篇系列答案
相关题目
7.铝热反应是铝的一个重要性质,该性质用途十分广泛,不仅被用于焊接钢轨,而且还常被用于冶炼高熔点的金属如钒、铬、锰等.

(1)某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图甲)进行铝热反应,现象很壮观.指明使用镁条和氯酸钾的目的是引发铝热反应.(不超过8个字)
(2)某同学用图乙装置进行铝热反应.取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液未见血红色.为测定该实验所得“铁块”中铁元素含量,设计实验流程如图所示.
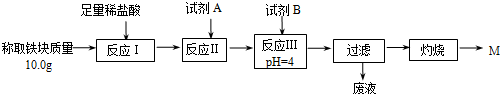
几种氢氧化物开始沉淀和完全沉淀的pH如下表所示.
①试剂A应选择C,试剂B应选择D.(填序号)
A.稀盐酸 B.氧化铁 C.H2O2溶液 D.氨水
②写出反应Ⅱ的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O
③设计简单实验证明M的成分是Fe2O3而非Fe3O4.
【限选试剂:稀盐酸、稀硫酸、氯水、高锰酸钾溶液、KSCN溶液、双氧水】
④上述实验应灼烧至M质量不变,则能证明M质量不变的标志是连续两次灼烧质量相差不大于0.1g.
⑤若最终红色粉未M的质量为12.0g,则该“铁块”的纯度是84%.

(1)某校化学兴趣小组同学,取磁性氧化铁按教材中的实验装置(如图甲)进行铝热反应,现象很壮观.指明使用镁条和氯酸钾的目的是引发铝热反应.(不超过8个字)
(2)某同学用图乙装置进行铝热反应.取反应后的“铁块”溶于盐酸,向其中滴加KSCN溶液,溶液未见血红色.为测定该实验所得“铁块”中铁元素含量,设计实验流程如图所示.

几种氢氧化物开始沉淀和完全沉淀的pH如下表所示.
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀时的pH | 7.5 | 2.8 | 4.2 | 9.6 |
| 沉淀完全时的pH | 9.0 | 4.0 | 5 | 11 |
A.稀盐酸 B.氧化铁 C.H2O2溶液 D.氨水
②写出反应Ⅱ的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O
③设计简单实验证明M的成分是Fe2O3而非Fe3O4.
【限选试剂:稀盐酸、稀硫酸、氯水、高锰酸钾溶液、KSCN溶液、双氧水】
| 操作 | 预期现象 |
| 取少量M固体于试管中,向其中加入足量稀硫酸;观察. | 固体完全溶解,溶液呈黄色. |
继续向上述溶液中滴入几滴(少量)高锰酸钾溶液,振荡观察 | 溶液紫红色未褪去 |
⑤若最终红色粉未M的质量为12.0g,则该“铁块”的纯度是84%.
8.下列实验操作或处理正确的是( )
| A. | 将NaOH溶液逐滴加入饱和的FeCl3溶液中制取Fe(OH)3胶体 | |
| B. | 氯气泄漏后应顺风向低处跑 | |
| C. | 金属钠着火立刻用湿布盖灭 | |
| D. | 做完焰色反应实验的铂丝用稀盐酸清洗 |
5.已知反应①KClO3+6HCl═3Cl2+KCl+3H2O②2KBrO3+Cl2═Br2+2KClO3③Cl2+2KBr═2KCl+Br2.
下列说法正确的是( )
下列说法正确的是( )
| A. | 上述三个反应都有单质生产,所以都是置换反应 | |
| B. | 氧化性由强到弱的顺序为KBrO3>KClO3>Cl2>Br2 | |
| C. | 反应①中还原剂与氧化剂的物质的量之比为6:1 | |
| D. | 若反应②中有1 mol还原剂参加反应,则氧化剂得电子的物质的量为2mol |
2.下列实验内容可以达到预期实验目的是( )
| 选项 | 实验内容 | 实验目的 |
| A | 将木炭与浓硫酸共热,得到的气体通入澄清石灰水 | 检验木炭的氧化产物是CO2 |
| B | 加入足量铁屑,充分反应后,过滤 | 除去FeCl2溶液中的少量FeCl3 |
| C | 将1mol CuSO4•5H2O溶解在1L水中 | 配制1mol/L的CuSO4溶液 |
| D | 将SO2通入酸性KMnO4溶液中 | 证明SO2具有漂白性 |
| A. | A | B. | B | C. | C | D. | D |
9.下列各物质中,不能由化合反应得到的是( )
| A. | FeCl3 | B. | FeCl2 | C. | Fe(OH)3 | D. | H2SiO3 |
6.化学与生活、社会密切相关.下列说法正确的是( )
| A. | 正常雨水的pH值为7.0,酸雨的pH值小于7.0 | |
| B. | 亚硝酸盐常做食品防腐剂,可以大量添加于食物中 | |
| C. | 自然界中的固氮作用对植物的生长有害无益 | |
| D. | 大量燃烧化石燃料是造成雾霾天气的重要原因之一 |