题目内容
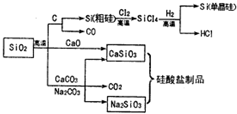 SiO2是一种化工原料,可以制备一系列物质.下列说法正确的是
SiO2是一种化工原料,可以制备一系列物质.下列说法正确的是( )
| A、图中所有反应都不属于氧化还原反应 | B、硅酸盐的化学性质稳定,常用于制造光导纤维 | C、可用盐酸除去石英砂(主要成分为SiO2)中少量的碳酸钙 | D、普通玻璃是由纯碱、石灰石和石英砂制成的,其熔点很高 |
分析:A.化学反应前后有元素化合价变化的一定是氧化还原反应;
B.光导纤维的成分是二氧化硅;
C.二氧化硅和盐酸不反应,碳酸钙溶于盐酸;
D.玻璃属于混合物,没有个固定的熔点.
B.光导纤维的成分是二氧化硅;
C.二氧化硅和盐酸不反应,碳酸钙溶于盐酸;
D.玻璃属于混合物,没有个固定的熔点.
解答:解:A.化学反应前后有元素化合价变化的一定是氧化还原反应,二氧化硅与碳反应生成硅单质的反应是氧化还原反应,故A错误;
B.光导纤维的成分是二氧化硅,不是硅酸盐,故B错误;
C.碳酸钙溶于盐酸生成氯化钙和水以及二氧化碳,二氧化硅和盐酸不反应,可以用盐酸除去石英(主要成分为SiO2)中混有的少量碳酸钙,故C正确;
D.玻璃是由纯碱、石灰石和石英制成的,玻璃属于混合物,没有固定的熔点,故D错误.
故选C.
B.光导纤维的成分是二氧化硅,不是硅酸盐,故B错误;
C.碳酸钙溶于盐酸生成氯化钙和水以及二氧化碳,二氧化硅和盐酸不反应,可以用盐酸除去石英(主要成分为SiO2)中混有的少量碳酸钙,故C正确;
D.玻璃是由纯碱、石灰石和石英制成的,玻璃属于混合物,没有固定的熔点,故D错误.
故选C.
点评:本题考查硅和二氧化硅的性质和用途,题目难度不大,注意只有纯净物有固定的熔沸点.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案
相关题目
CaCO3是一种化工原料,可以通过反应生成一系列物质,如图所示.

下列说法正确的是( )

下列说法正确的是( )
| A、Cl2和SO2均可以漂白有色物质,且漂白的原理相同 | ||||
B、由SiO2+Na2CO3
| ||||
| C、工业上,可先向饱和食盐水中通入NH3后再通入CO2制NaHCO3 | ||||
| D、制取玻璃、纯碱和漂白粉所涉及的反应都是非氧化还原反应 |
SiO2是一种化工原料,可以制备一系列物质(如图).下列说法错误的是( )
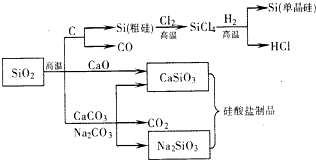

| A、图所含反应都不属于氧化还原反应 | B、纯净的二氧化硅和单晶硅都是信息产业的重要基础材料 | C、用盐酸可除去石英砂(主要成分为SiO2)中少量的碳酸钙 | D、高炉炼铁时用石灰石将铁矿石中的脉石转化为易熔的炉渣 |


 Na2SiO3+CO2↑可知,H2CO3的酸性强于H2SiO3
Na2SiO3+CO2↑可知,H2CO3的酸性强于H2SiO3