题目内容
16. W、X、Y、Z分别为H、C、N、O元素
W、X、Y、Z分别为H、C、N、O元素(1)由XW4、Z2和KOH溶液组成的新型燃料电池中,负极上发生反应的电极反应式为CH4-8e-+10OH-═CO32-+7H2O
(2)已知:2YZ2(g)?Y2Z4(g)△H<0.在恒温恒容条件下,将一定量YZ2和Y2Z4的混合气体通入容积为2L的密闭容器中,反应过程中各物质的物质的量浓度c随时间t的变化关系如图所示.
①a、b、c、d四个点中,化学反应处于平衡状态的是点bd.
②25min时,增加了NO2(填物质的化学式)0.8 mol.
分析 (1)由CH4、O2和KOH溶液组成的新型燃料电池,负极上发生氧化反应,甲烷在负极失去电子,碱性条件下生成碳酸根离子与水;
(2)①物质的浓度不发生变化时表示化学反应处于平衡状态;
②由图象曲线变化可知,在10min时,N浓度变化量为0.4mol/L,M浓度变化量为0.2mol/L,则N为NO2的变化曲线,M为N2O4的变化曲线,25min瞬间,N2O4的浓度不变,NO2的浓度变为1mol/L,应是加入NO2,根据浓度变化量计算加入NO2的物质的量.
解答 解:(1)由CH4、O2和KOH溶液组成的新型燃料电池,负极上发生氧化反应,甲烷在负极失去电子,碱性条件下生成碳酸根离子与水,负极电极反应式为:CH4-8e-+10OH-═CO32-+7H2O,
故答案为:CH4-8e-+10OH-═CO32-+7H2O;
(2)①物质的浓度不发生变化时表示化学反应处于平衡状态,由图可知,处于平衡状态的点是b和d,
故选:bd;
②由图象曲线变化可知,在10min时,N浓度变化量为0.4mol/L,M浓度变化量为0.2mol/L,则N为NO2的变化曲线,M为N2O4的变化曲线,25min瞬间,N2O4的浓度不变,NO2的浓度变为1mol/L,应是加入NO2,ze 加入NO2的物质的量2L×(1mol/L-0.6mol/L)=0.8mol,
故答案为:NO2;0.8.
点评 本题考查化学平衡图象、原电池,明确图象中纵横坐标及点、线、面的意义,关键是判断N、M所代表的物质,难度中等.

练习册系列答案
相关题目
6.如图装置进行相应的实验,能达到实验目的是( )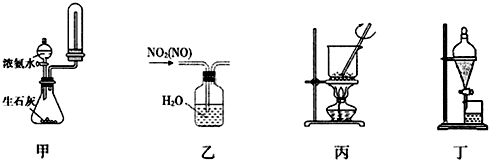

| A. | 用装置甲制取并收集干燥纯净的NH3 | |
| B. | 用装置乙除去NO2中混有的少量NO | |
| C. | 用装置丙将氢氧化钠固体加热熔融 | |
| D. | 用装置丁把溴水中的溴萃取分离出来 |
11.反应A(g)+3B(g)═2C(g)+2D(g)在不同情况下测得反应速率,其中反应最快的是( )
| A. | v(A)=0.5mol(L•min) | B. | v(B)=0.9mol(L•min) | C. | v(C)=1.2mol(L•min) | D. | v(D)=0.4mol(L•min) |
1.某溶液中含K+、Fe3+、Fe2+、Cl-、CO32-、NO3-、SO42-、SiO32-、I-中的若干种,某同学欲探究该溶液的组成,进行如下实验:
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰.
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成.
Ⅲ.取Ⅱ反应后的溶液分别置于两支试管中,第一支试管中加入BaCl2溶液,有白色沉淀生成,再滴加KSCN溶液,上层清液变红;第二支试管中加入CCl4,充分振荡静置后溶液分层,下层为无色.
下列说法正确的是( )
Ⅰ.用铂丝蘸取少量溶液,在火焰上灼烧,透过蓝色钴玻璃,观察到紫色火焰.
Ⅱ.另取原溶液加入足量盐酸有无色气体生成,该气体遇空气变成红棕色,此时溶液颜色加深,但无沉淀生成.
Ⅲ.取Ⅱ反应后的溶液分别置于两支试管中,第一支试管中加入BaCl2溶液,有白色沉淀生成,再滴加KSCN溶液,上层清液变红;第二支试管中加入CCl4,充分振荡静置后溶液分层,下层为无色.
下列说法正确的是( )
| A. | 原溶液中肯定不含Fe2+、NO3-、SiO32-、I- | |
| B. | 原溶液中肯定含有K+、Fe3+、Fe2+、NO3-、SO42- | |
| C. | 步骤Ⅱ中无色气体是NO气体,无CO2气体产生 | |
| D. | 为确定是否含有Cl-,可取原溶液加入过量硝酸银溶液,观察是否产生白色沉淀 |
5.滨海新区8.12爆炸事故给我们敲响了安全的警钟,对危险化学品要在包装上有警示标志.下列化学药品与其危险化学品图形标志不一致的一组是( )
| A. |  硫磺 | B. |  高锰酸钾 | C. |  氢气 | D. |  乙醇 |
6.某校兴趣小组对SO2与新制Cu(OH)2悬浊液的反应进行探究,实验如表:
(1)制取新制Cu(OH)2悬浊液的离子方程式为Cu2++2OH-═Cu(OH)2↓.
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净.向洗净后的Cu(OH)2中加入5mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明:黄色沉淀消失生成大量白色沉淀(或实验II与实验I的现象差异)与Cl-有关(或与SO42-无关).检验Cu(OH)2洗涤干净的方法是取最后一次洗涤液于试管中,向其中滴加少量硝酸酸化的AgNO3溶液,不出现白色沉淀,证明Cu(OH)2洗涤干净.
(3)同学们对白色沉淀的成分继续进行探究.查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸.它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液.
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl+2NH3•H2O=Cu(NH3)2++Cl-+2H2O、4Cu(NH3)2++8NH3•H2O+O2═4Cu(NH3)42++4OH-+6H2O.
②乙同学用另一种方法证明了该白色沉淀为CuCl,实验方案如图:
填写如表空格:
③写出实验II中由Cu(OH)2生成白色沉淀的离子方程式:2Cu(OH)2+2Cl-+SO2═2CuCl↓+SO42-+2H2O.
(4)丙同学通过实验证明实验Ⅰ中观察到的砖红色沉淀是Cu2O.完成合理的实验方案:取少量Cu2O固体于试管中,加5mL蒸馏水,向其中持续通入SO2,一段时间后,静置,试管底部有少量紫红色固体,溶液呈绿色(或现象与实验I相同),则说明砖红色沉淀是Cu2O.
| 装置 | 序号 | 试管中的药品 | 现象 |
持续通入  | 实验Ⅰ | 1.5mL 1mol?L-1 CuSO4溶液和3.5mL 1mol?L-1 NaOH溶液混合 | 开始时有砖红色沉淀出现,一段时间后,砖红色沉淀消失,静置,试管底部有少量紫红色固体,溶液呈绿色 |
实验Ⅱ | 1.5mL 1mol?L-1 CuCl2溶液和3.5mL 1mol?L-1 NaOH溶液混合 | 开始时有黄色沉淀出现,一段时间后,黄色沉淀消失,静置,生成大量白色沉淀,溶液呈绿色 |
(2)甲同学重新用实验II的方法制备新制Cu(OH)2悬浊液,过滤,用蒸馏水洗涤干净.向洗净后的Cu(OH)2中加入5mL蒸馏水,再持续通入SO2气体,现象与实验I相同,此步实验证明:黄色沉淀消失生成大量白色沉淀(或实验II与实验I的现象差异)与Cl-有关(或与SO42-无关).检验Cu(OH)2洗涤干净的方法是取最后一次洗涤液于试管中,向其中滴加少量硝酸酸化的AgNO3溶液,不出现白色沉淀,证明Cu(OH)2洗涤干净.
(3)同学们对白色沉淀的成分继续进行探究.查阅资料如下:CuCl为白色固体,难溶于水,能溶于浓盐酸.它与氨水反应生成Cu(NH3)2+,在空气中会立即被氧化成含有蓝色Cu(NH3)42+溶液.
①甲同学向洗涤得到的白色沉淀中加入氨水,得到蓝色溶液,此过程中反应的离子方程式为:CuCl+2NH3•H2O=Cu(NH3)2++Cl-+2H2O、4Cu(NH3)2++8NH3•H2O+O2═4Cu(NH3)42++4OH-+6H2O.
②乙同学用另一种方法证明了该白色沉淀为CuCl,实验方案如图:

填写如表空格:
| 试剂1 | 试剂2 | 蒸馏水 | |
| 现象1 | 现象2 |
(4)丙同学通过实验证明实验Ⅰ中观察到的砖红色沉淀是Cu2O.完成合理的实验方案:取少量Cu2O固体于试管中,加5mL蒸馏水,向其中持续通入SO2,一段时间后,静置,试管底部有少量紫红色固体,溶液呈绿色(或现象与实验I相同),则说明砖红色沉淀是Cu2O.
