题目内容
9.为了说明影响化学反应快慢的因素,甲、乙、丙、丁四位同学分别设计了如下A-D四个实验,你认为结论不正确的是( )| A. | 在相同条件下,等质量的大理石块和大理石粉与相同浓度的盐酸反应时,粉状的反应速率快 | |
| B. | 将相同大小、相同面积的镁条和铝条与相同浓度的盐酸反应,前者速率大于后者 | |
| C. | 两支试管中分别加入相同质量的氯酸钾,其中一支试管中再加入少量二氧化锰,同时加热,产生氧气的快慢不同 | |
| D. | 将铜片放入稀硫酸中,无现象.若再向所得溶液中加入硝酸银溶液,一段时间后,由于形成原电池,可看到有氢气生成 |
分析 A.固体的表面积不同,化学反应速率不同;
B.不同的金属,性质不同,为影响化学反应速率的主要因素;
C.催化剂能加快反应速率;
D.铜不能置换出氢气.
解答 解:A.固体的表面积不同,化学反应速率不同,粉末状固体的表面积比块状固体表面积大,反应速率大,故A正确;
B.镁条和铝条的活泼性不同,与相同浓度盐酸反应,镁反应速率较大,故B正确;
C.催化剂能加快反应速率,在氯酸钾分解的试验中,二氧化锰起到催化剂的作用,故C正确;
D.铜为不活泼金属,与稀硫酸不反应,故D错误.
故选D.
点评 本题考查外界条件对化学反应速率的影响,题目难度不大,注意B项,为易错点,物质的性质是影响化学反应速率的主要因素.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.某同学在实验室进行以下实验,请将实验①②③的现象和离子反应方程式填入实验报告中.


| 编号 | 现象 | 离子方程式 |
| ① | ||
| ② | ||
| ③ |
14.下列各组物质在溶液中能大量共存的是( )
| A. | FeCl3 Na2SO4 HCl | B. | NaOH NaCl HNO3 | ||
| C. | CuSO4 NaNO3 KOH | D. | Na2CO3 HCl Ca(OH)2 |
18. 科学家对石墨进行处理,使得石墨片的厚度逐渐减少,最终获得目前已知的最薄的材料--石墨烯(如图).下列关于石墨烯的说法正确的是( )
科学家对石墨进行处理,使得石墨片的厚度逐渐减少,最终获得目前已知的最薄的材料--石墨烯(如图).下列关于石墨烯的说法正确的是( )
 科学家对石墨进行处理,使得石墨片的厚度逐渐减少,最终获得目前已知的最薄的材料--石墨烯(如图).下列关于石墨烯的说法正确的是( )
科学家对石墨进行处理,使得石墨片的厚度逐渐减少,最终获得目前已知的最薄的材料--石墨烯(如图).下列关于石墨烯的说法正确的是( )| A. | 石墨烯是一新型的纳米化合物 | B. | 石墨烯与C60互为同素异形体 | ||
| C. | 石墨烯是一种有机物 | D. | 石墨烯中碳元素的化合价为+3 |
19.下列有关实验设计或对实验原理的描述正确的是( )
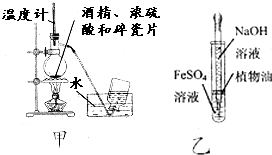

| A. | 为测定熔融氢氧化钠的导电性,可在瓷坩埚中熔化氢氧化钠固体 | |
| B. | 用甲图装置制取乙烯 | |
| C. | 用乙图装置制备少量氢氧化亚铁 | |
| D. | 加入适量乙醇和浓硫酸,加热,可除去乙酸乙酯中少量的乙酸 |
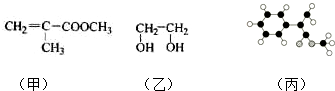

 ;
;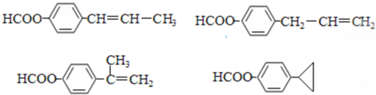 (只写一种即可)
(只写一种即可)