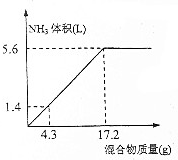
题目内容
1.下列表示对应化学反应的离子方程式正确的是( )| A. | Fe2O3溶于HI溶液中:Fe2O3+6H+═2Fe3++3H2O | |
| B. | 明矾溶于水产生Al(OH)3胶体:Al3++3H2O═Al(OH)3↓+3H+ | |
| C. | Na2O与水反应:O2-+H2O═2OH- | |
| D. | Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-═CaCO3↓+H2O |
分析 A.发生氧还原反应生成碘化亚铁、碘和水;
B.水解为可逆反应,且不生成沉淀;
C.氧化钠在离子反应中保留化学式;
D.NaOH完全反应,生成碳酸钙、碳酸氢钠和水.
解答 解:A.Fe2O3溶于HI溶液中的离子反应为2I-+Fe2O3+6H+═2Fe2++I2+3H2O,故A错误;
B.明矾溶于水产生Al(OH)3胶体的离子反应为Al3++3H2O?Al(OH)3(胶体)+3H+,故B错误;
C.Na2O与水反应的离子反应为Na2O+H2O═2OH-+2Na+,故C错误;
D.Ca(HCO3)2溶液与少量NaOH溶液反应的离子反应为HCO3-+Ca2++OH-═CaCO3↓+H2O,故D正确;
故选D.
点评 本题考查离子反应方程式的书写,为高频考点,把握发生的反应、离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,题目难度不大.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案
相关题目
11.下列化学用语描述正确的是( )
| A. | CO2的电子式?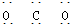 ? ? | B. | Cl-的结构示意图 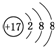 | ||
| C. | 乙烯的电子式C2H4 | D. | 质量数为37的氯原子${\;}_{37}^{17}$Cl |
12.现有①、②、③三种元素的基态原子的电子排布式如下:①1s22s22p63s2; ②1s22s22p63s23p1;③1s22s22p3;④1s22s22p4.则下列有关比较中不正确的是( )
| A. | 电负性:④>③>②>① | B. | 最高正化合价:③>①>②>④ | ||
| C. | 原子半径:①>②>③>④ | D. | 第一电离能:④>③>②>① |
16.医学研究证明,用放射性${\;}_{53}^{135}$Ⅰ治疗肿瘤可收到一定疗效,下列有关${\;}_{53}^{135}$Ⅰ的叙述正确的是( )
| A. | 核内的中子数为53 | |
| B. | 核内的电子数为135 | |
| C. | 核内的中子数与核外电子数之差为29 | |
| D. | 质量数为82 |
13.X、Y、Z、W均为短周期元素,原子序数依次递增.X与W位于同一主族,Y、Z、W同周期,Z原子的最外层电子数是最内层电子数的3倍,Y、Z、W原子的最外层电子数之和为15.下列说法正确的是( )
| A. | X的最高价氧化物对应水化物的酸性大于W | |
| B. | Z的气态氢化物的稳定性大于W | |
| C. | YZ和ZW2所含化学键类型相同 | |
| D. | 简单离子半径:r(Y2+)<r(X-)<r(W-)<r(Z2-) |
12.某有机物的结构简式为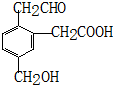 ,它在一定条件下能发生的反应有①加成反应 ②水解反应 ③酯化反应 ④氧化反应 ⑤中和反应 ⑥消去反应( )
,它在一定条件下能发生的反应有①加成反应 ②水解反应 ③酯化反应 ④氧化反应 ⑤中和反应 ⑥消去反应( )
 ,它在一定条件下能发生的反应有①加成反应 ②水解反应 ③酯化反应 ④氧化反应 ⑤中和反应 ⑥消去反应( )
,它在一定条件下能发生的反应有①加成反应 ②水解反应 ③酯化反应 ④氧化反应 ⑤中和反应 ⑥消去反应( )| A. | ②③④ | B. | ①③④⑤ | C. | ①③⑤⑥ | D. | ②③④⑤⑥ |
 .
. ,该氢化物的水溶液显碱性(填“酸性”、“碱性”或“中性”),该溶液与少量AlCl3溶液反应的离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
,该氢化物的水溶液显碱性(填“酸性”、“碱性”或“中性”),该溶液与少量AlCl3溶液反应的离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+.