题目内容
下列关于常见有机化合物的说法中,正确的是( )
| A、乙烯和聚乙烯都能与溴的四氯化碳溶液发生加成反应 |
| B、蔗糖和麦芽糖的水解产物都是葡萄糖 |
| C、石油经过分馏得到的各种产物是不同温度范围内的混合物 |
| D、苯和苯乙烯的最简式相同,是同系物 |
考点:有机物的结构和性质
专题:有机物的化学性质及推断
分析:A.聚乙烯不含碳碳双键;
B.蔗糖水解生成葡萄糖和果糖;
C.石油分馏可得得到汽油、煤油等分馏产品;
D.苯和苯乙烯的结构不同;
B.蔗糖水解生成葡萄糖和果糖;
C.石油分馏可得得到汽油、煤油等分馏产品;
D.苯和苯乙烯的结构不同;
解答:
解:A.聚乙烯为加聚产物,不含碳碳双键,不能与溴发生加成反应,故A错误;
B.蔗糖水解生成葡萄糖和果糖,故B错误;
C.分馏石油得到的各个馏分中含有多种烃类物质,是混合物,如汽油主要成分为C4~C12脂肪烃和环烃类,故C正确;
D.苯和苯乙烯的结构不同,苯乙烯含有碳碳双键,而苯不含,二者结构不同,不是同系物,故D错误.
故选C.
B.蔗糖水解生成葡萄糖和果糖,故B错误;
C.分馏石油得到的各个馏分中含有多种烃类物质,是混合物,如汽油主要成分为C4~C12脂肪烃和环烃类,故C正确;
D.苯和苯乙烯的结构不同,苯乙烯含有碳碳双键,而苯不含,二者结构不同,不是同系物,故D错误.
故选C.
点评:本题综合考查有机物的结构和性质,为高频考点,侧重于学生的分析能力和基础知识的综合理解和运用的考查,难度不大,注意相关知识的积累.

练习册系列答案
相关题目
青霉氨基酸的结构式如图所示为它不能发生的反应是( )
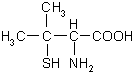
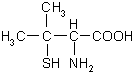
| A、能与NaOH发生中和反应 |
| B、能与醇发生酯化反应 |
| C、能与盐酸反应生成盐 |
| D、能发生银镜反应 |
安全教育是化学教育的重要内容.根据你掌握的知识判断,下列各项中符合安全操作要求的是( )
①在加油站内拨打手机
②在煤矿巷道内用明火照明
③闻氯气的气味时,用手轻轻在瓶口扇动,仅使极少量的氯气飘进鼻孔
④为了节约药品,锌与稀硫酸一开始反应,就做氢气点燃实验
⑤稀释浓硫酸时,沿烧杯内壁将浓硫酸缓缓加入水中,边加边搅拌
⑥不慎将酒精灯打翻在桌上失火时,立即用湿抹布盖灭
⑦不慎将酸液溅到眼中,应立即用水冲洗,边洗边眨眼睛
⑧不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液.
①在加油站内拨打手机
②在煤矿巷道内用明火照明
③闻氯气的气味时,用手轻轻在瓶口扇动,仅使极少量的氯气飘进鼻孔
④为了节约药品,锌与稀硫酸一开始反应,就做氢气点燃实验
⑤稀释浓硫酸时,沿烧杯内壁将浓硫酸缓缓加入水中,边加边搅拌
⑥不慎将酒精灯打翻在桌上失火时,立即用湿抹布盖灭
⑦不慎将酸液溅到眼中,应立即用水冲洗,边洗边眨眼睛
⑧不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液.
| A、③⑤⑥⑦⑧ | B、①②④ |
| C、①②⑥⑦⑧ | D、③④⑤⑦⑧ |
下列各组物质既不是同系物又不是同分异构体的是( )
| A、软脂酸和硬脂酸 |
| B、甲酸甲酯和乙酸 |
| C、油酸和乙酸 |
| D、对甲基苯酚和苯甲醇 |
使石蕊试液变红的某透明溶液中,下列各组离子能大量共存的是( )
| A、CO32-、Na+、K+、OH- |
| B、Ba2+、CO32-、NO3-、SO42- |
| C、K+、Cu2+、Cl-、SO42- |
| D、Fe2+、NO3-、Cl-、SO42- |


 (苯胺,易被氧化)
(苯胺,易被氧化) 的说法正确的是
的说法正确的是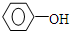 ;④CH3COOC2H5;⑤CH3COOH五物质中:
;④CH3COOC2H5;⑤CH3COOH五物质中: