题目内容
能正确表示下列反应的离子方程式是( )
| A、将Cl2通入氯化亚铁溶液:Fe2++Cl2═Fe3++2Cl- |
| B、氯气通入水中:Cl2+H2O═H++Cl-+ClO- |
| C、AlCl3溶液中通入过量的氨水:Al3++3NH3?H2O═Al(OH)3↓+3NH4+ |
| D、Cl2通入烧碱溶液中:Cl2+OH-═Cl-+ClO-+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.根据电荷守恒判断,该离子方程式两边电荷不守恒;
B.次氯酸为弱电解质,离子方程式中次氯酸不能拆开,且不明显电荷守恒;
C.氨水为弱碱,不会溶解氢氧化铝,氯化铝与氨水反应生成氢氧化铝沉淀;
D.根据电荷守恒判断,离子方程式两边不满足电荷守恒.
B.次氯酸为弱电解质,离子方程式中次氯酸不能拆开,且不明显电荷守恒;
C.氨水为弱碱,不会溶解氢氧化铝,氯化铝与氨水反应生成氢氧化铝沉淀;
D.根据电荷守恒判断,离子方程式两边不满足电荷守恒.
解答:
解:A.将Cl2通入氯化亚铁溶液,离子方程式必须满足电荷守恒,正确的离子方程式为:2Fe2++Cl2═2Fe3++2Cl-,故A错误;
B.氯气通入水中,次氯酸不能拆开,正确的离子方程式为:Cl2+H2O═H++Cl-+HClO,故B错误;
C.AlCl3溶液中通入过量的氨水,反应生成氢氧化铝沉淀,反应的离子方程式为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+,故C正确;
D.氯气通入烧碱溶液中,反应生成氯化钠、次氯酸钠和水,离子方程式必须满足电荷守恒,正确的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故D错误;
故选C.
B.氯气通入水中,次氯酸不能拆开,正确的离子方程式为:Cl2+H2O═H++Cl-+HClO,故B错误;
C.AlCl3溶液中通入过量的氨水,反应生成氢氧化铝沉淀,反应的离子方程式为:Al3++3NH3?H2O═Al(OH)3↓+3NH4+,故C正确;
D.氯气通入烧碱溶液中,反应生成氯化钠、次氯酸钠和水,离子方程式必须满足电荷守恒,正确的离子方程式为:Cl2+2OH-═Cl-+ClO-+H2O,故D错误;
故选C.
点评:本题考查了离子方程式的书写判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等).

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
短周期元素甲、乙、丙、丁的原子序数依次增大,甲和乙形成的气态化合物的水溶液呈碱性,乙位于第VA族,甲和丙同主族,丁的最外层电子数和电子层数相等,则( )
| A、原子半径:丙<丁<乙 |
| B、乙、丙、丁的最高价氧化物对应的水化物能相互反应 |
| C、甲、乙、丙的氧化物均为共价化合物 |
| D、单质的还原性:丁>丙>甲 |
近两年流行喝苹果醋,苹果醋是一种由苹果发酵而成的具有解毒、降脂、减肥和止泻等明显药效的健康食品.苹果酸(α-羟基丁二酸)是这种饮料的主要酸性物质,苹果酸的结构简式为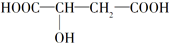 ,下列说法不正确的是( )
,下列说法不正确的是( )
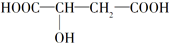 ,下列说法不正确的是( )
,下列说法不正确的是( )| A、苹果酸在一定条件下能发生酯化反应 |
| B、苹果酸在一定条件下能发生催化氧化反应 |
| C、苹果酸1 mol能与3 mol Na反应 |
| D、1 mol苹果酸与Na2CO3溶液反应最多消耗3 mol Na2CO3 |
下列说法中正确的是( )
| A、PCl3分子是三角锥形,这是因为P原子是以sp3杂化的结果 |
| B、凡中心原子采取sp3杂化的分子,其几何构型都是四面体形 |
| C、sp3杂化轨道是由任意的1个s轨道和3个p轨道混合形成的四个sp3杂化轨道 |
| D、AB3型的分子空间构型必为平面三角形 |
稗草烯是一种选择性内吸传导性除草剂.其结构简式为  下列说法中不正确的是( )
下列说法中不正确的是( )
 下列说法中不正确的是( )
下列说法中不正确的是( )| A、该物质能使溴水褪色 |
| B、该物质属于烯烃 |
| C、1 mol该有机物最多可与4mol H2发生加成反应 |
| D、该物质在一定条件下可发生加聚反应 |
下列各组化合物均属于烃的衍生物且只用水就可以区分的是( )
A、 与 与 |
B、 与 与 |
| C、CH2BrCH2Br与CH3CH2OH |
D、 |
将pH=13的NaOH溶液平均分成两份,一份加适量水,另一份加入与该NaOH溶液物质的量浓度相同的适量硫酸后,pH都降低了1,则加入的水与硫酸的体积比为( )
| A、10:1 | B、11:1 |
| C、20:1 | D、21:1 |
含有2~5个碳原子的直链烷烃沸点和燃烧热的数据见下表:
*燃烧热:1mol物质完全燃烧,生成二氧化碳、液态水时所放出的热量.
根据表中数据,下列判断错误的是( )
| 烷烃名称 | 乙烷 | 丙烷 | 丁烷 | 戊烷 |
| 沸点/℃ | -88.6 | -42.1 | -0.5 | 36.1 |
| *燃烧热/kJ?mol-1 | 1 560.7 | 2 219.2 | 2 877.6 | 3 535.6 |
根据表中数据,下列判断错误的是( )
| A、正庚烷在常温常压下肯定不是气体 |
| B、随碳原子数增加,烷烃沸点和燃烧热都成比例增加 |
| C、随碳原子数增加,烷烃沸点逐渐升高 |
| D、烷烃燃烧热随所含碳原子数增加而增加 |