题目内容
A、B、C、D四种金属分别用导线两两相连浸入电解液中组成原电池。A、B相连时,A为负极;C、D相连时,电流由D流到C;A、C 相连时,C极上有大量气泡;B、D相连时,D极发生氧化反应。据此判断四种金属的活动性顺序是
- A.A>C>D>B
- B.D>A>B>C
- C.A>D>C>B
- D.C>B>A>D
A
解析:
在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。A、B相连时,A为负极,则金属性是A大于B。C、D相连时,电流由D流到C,则金属性是C大于D。A、C 相连时,C极上有大量气泡,所以金属性是A大于C。B、D相连时,D极发生氧化反应,则金属性是D大于B,答案选A。
解析:
在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。A、B相连时,A为负极,则金属性是A大于B。C、D相连时,电流由D流到C,则金属性是C大于D。A、C 相连时,C极上有大量气泡,所以金属性是A大于C。B、D相连时,D极发生氧化反应,则金属性是D大于B,答案选A。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
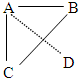 若A、B、C、D四种元素位于元素周期表中如右图所示位置,请回答以下问题:
若A、B、C、D四种元素位于元素周期表中如右图所示位置,请回答以下问题: