题目内容
16.下列关于电解质溶液的正确判断是( )| A. | 加水稀释,氨水溶液中导电粒子的数目减少 | |
| B. | 通入HCl气体,氨水溶液中NH3•H2O的电离平衡向右移动,溶液的pH增大 | |
| C. | 由0.1mol/L一元碱BOH溶液的 pH=10,可推知BOH溶液中存在BOH═B++OH- | |
| D. | 由0.1mol/L一元酸HA溶液的 pH=3,可推知NaA溶液中存在A-+H2O═HA+OH- |
分析 A.加水稀释后,溶液中c(H+)增大;
B.通入HCl气体,氨水溶液中NH3•H2O的电离平衡向右移动,氢离子浓度增大,溶液的pH减小;
C.0.1mol/L一元碱BOH溶液的pH=10,溶液中氢氧根离子浓度小于BOH浓度,则BOH为弱碱;
D.在0.1mol/L一元酸HA溶液的pH=3,则HA为弱酸,NaA为强碱弱酸盐.
解答 解:A.加水稀释后,溶液中c(NH4+)、c(OH-)减小,温度不变,离子积常数不变,则c(H+)增大,故A错误;
B.通入HCl气体,氨水溶液中NH3•H2O的电离平衡向右移动,氢离子浓度增大,溶液的pH减小,故B错误;
C.0.1mol/L一元碱BOH溶液的pH=10,溶液中氢氧根离子浓度小于BOH浓度,则BOH为弱碱,则BOH溶液中存在BOH?B++OH-,故C错误;
D.在0.1mol/L一元酸HA溶液的pH=3,则HA为弱酸,NaA为强碱弱酸盐,水解呈碱性,水解方程式为A-+H2O?HA+OH-,故D正确;
故选D.
点评 本题考查弱电解质的电离、盐类水解等知识点,侧重考查弱电解质电离的知识点,明确弱电解质的电离,综合性强,但比较容易.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
19.某溶液中有Mg2+、Fe2+、Cu2+三种离子,向其中加入过量的NaOH溶液后过滤,将滤渣高温灼烧并将灼烧后的固体投入过量的稀盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是( )
| A. | Mg2+ | B. | Fe2+ | C. | Cu2+ | D. | 无减少 |
11.现有几组物质的熔点数据如下表:
据此回答下列问题:
(1)A组属于原子晶体晶体,其熔化时克服的微粒间的作用力是共价键;
(2)B组晶体共同的物理性质是①②③④(填序号);①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于HF分子间存在氢键;
(4)D组晶体可能具有的性质是②④(填序号);①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电.
| A组 | B组 | C组 | D组 |
| 金刚石:3110℃ | Li:181℃ | HF:-83℃ | NaCl:801℃ |
| 硅晶体:1410℃ | Na:98℃ | HCl:-114℃ | KCl:776℃ |
| 硼晶体:2300℃ | K:64℃ | HBr:-89℃ | RbCl:718℃ |
| 二氧化硅:1723℃ | Rb:39℃ | HI:-51℃ | CsCl:645℃ |
(1)A组属于原子晶体晶体,其熔化时克服的微粒间的作用力是共价键;
(2)B组晶体共同的物理性质是①②③④(填序号);①有金属光泽 ②导电性 ③导热性 ④延展性
(3)C组中HF熔点反常是由于HF分子间存在氢键;
(4)D组晶体可能具有的性质是②④(填序号);①硬度小 ②水溶液能导电 ③固体能导电 ④熔融状态能导电.
6.下列表示物质结构的化学用语正确的是( )
| A. | CH4分子的比例模型: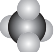 | B. | CO2的电子式:O::C::O | ||
| C. | Cl-的离子结构示意图: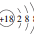 | D. | 中子数为18的硫原子:${\;}_{16}^{18}$S |

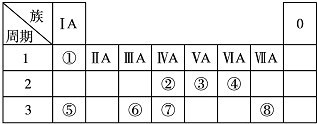
 ,
,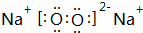 .若用球棍模型表示①和④形成的化合物的分子结构,应该是下图中的B.
.若用球棍模型表示①和④形成的化合物的分子结构,应该是下图中的B.