题目内容
下列关于胶体的叙述不正确的是( )
| A、胶体区别于其他分散系的本质特征是分散质的微粒直径在10-9~10-7m之间 |
| B、胶体的分散质粒子可以通过滤纸孔隙,所以可以通过过滤操作分离溶液和胶体 |
| C、用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象不相同 |
| D、Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的 |
考点:胶体的重要性质
专题:溶液和胶体专题
分析:A、根据胶体区别于其他分散系的本质特征是分散质的微粒直径大小;
B、根据溶液和胶体都能通过滤纸分析;
C、根据溶液不具有丁达尔效应,而胶体具有丁达尔效应,
D、根据Fe(OH)3 胶体的表面积较大,能吸附水中悬浮的固体颗粒达到净水的目的.
B、根据溶液和胶体都能通过滤纸分析;
C、根据溶液不具有丁达尔效应,而胶体具有丁达尔效应,
D、根据Fe(OH)3 胶体的表面积较大,能吸附水中悬浮的固体颗粒达到净水的目的.
解答:
解:A、胶体区别于其他分散系的本质特征是分散质的微粒直径大小,胶体分散系的微粒直径在1~100nm之间,故A正确;
B、胶体的分散质粒子可以通过滤纸孔隙,溶液液能通过,不能通过过滤操作分离溶液和胶体,胶体不能通过半透膜,可以通过渗析方法分离溶液和胶体,故B错误;
C、NaCl溶液不具有丁达尔效应,而Fe(OH)3胶体具有丁达尔效应,现象不相同,故C正确;
D、Fe(OH)3 胶体的表面积较大,能吸附水中悬浮的固体颗粒达到净水的目的,故D正确;
故选B.
B、胶体的分散质粒子可以通过滤纸孔隙,溶液液能通过,不能通过过滤操作分离溶液和胶体,胶体不能通过半透膜,可以通过渗析方法分离溶液和胶体,故B错误;
C、NaCl溶液不具有丁达尔效应,而Fe(OH)3胶体具有丁达尔效应,现象不相同,故C正确;
D、Fe(OH)3 胶体的表面积较大,能吸附水中悬浮的固体颗粒达到净水的目的,故D正确;
故选B.
点评:本题考查学生胶体的特性以及溶液和胶体的本质区别,较简单,熟悉胶体的性质是解答的关键.

练习册系列答案
相关题目
下列反应中符合H++OH-=H2O离子反应的是( )
| A、稀硫酸与稀氨水 |
| B、稀硫酸与氢氧化钡溶液 |
| C、稀硝酸与氢氧化钡溶液 |
| D、盐酸与氢氧化铁反应 |
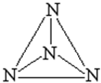 意大利科学家获得了极具研究价值的N4(分子结构如图所示),以下有关物质结构的说法正确的是( )
意大利科学家获得了极具研究价值的N4(分子结构如图所示),以下有关物质结构的说法正确的是( )| A、N均是以SP3杂化,N-N均为σ键 |
| B、N的电负性大于O,所以NH3的沸点低于H2O |
| C、N4为原子晶体,每个N的配位数为3 |
| D、N原子核外有5个未成对电子 |
下列对化学反应速率(υ)说法正确的是( )
| A、随着反应物浓度增大,活化分子百分数增加,υ增大 |
| B、催化剂降低活化能,使活化分子百分数增加,υ增大 |
| C、在使用酶催化剂时,大幅度提高反应温度可更好地提高υ |
| D、只要反应中有固体、液体物质,压强的变化对υ的影响可以忽略不计 |
下列各组物质,属于电解质的是( )
| A、NaCl |
| B、铜 |
| C、蔗糖 |
| D、CO2 |
同温同压下,含相同原子数的下列气体,密度最大的是( )
| A、SO2 |
| B、CO2 |
| C、HCl |
| D、CH4 |
下列说法不正确的是( )
| A、手机上用的锂离子电池属于二次电池 |
| B、测定中和反应的反应热,需要记录体系达到的最终温度 |
| C、催化剂能加快化学反应速率是因为降低了反应的活化能,增大了活化分子百分率 |
| D、温度对化学平衡的影响是通过改变平衡常数实现的 |
化学是一门实用性强的自然科学,在社会、生产、生活中起着重要的作用,下列说法正确的是( )
| A、金属钠具有强还原性,可用与TiCl4溶液反应制取金属Ti |
B、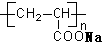 表示一种吸水性高分子树脂 表示一种吸水性高分子树脂 |
| C、用于现代建筑的钢筋混凝土不属于复合材料 |
| D、山东东营广饶县一男子收到网购物品后,因吸入氟乙酸甲酯中毒身亡,氟乙酸甲酯的结构简式为FCH2COOCH3,能与H2发生加成反应,也能被LiAlH4还原 |