题目内容
下列排列顺序错误的是( )
| A、酸性:H4SiO4<H3PO4<H2SO4<HClO4 |
| B、碱性:Ca(OH)2>Mg(OH)2>Al(OH)3 |
| C、原子半径:F<O<S<Na |
| D、氢化物的稳定性:H2S>H2O>HF |
考点:非金属在元素周期表中的位置及其性质递变的规律,金属在元素周期表中的位置及其性质递变的规律
专题:元素周期律与元素周期表专题
分析:A.元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强;
B.元素的金属性越强,对应的最高价氧化物的水化物的碱性越强;
C.根据同周期元素从左到右原子半径逐渐减小,同主族元素从上到下原子半径逐渐增大判断;
D.元素的非金属性越强,对应的氢化物越稳定.
B.元素的金属性越强,对应的最高价氧化物的水化物的碱性越强;
C.根据同周期元素从左到右原子半径逐渐减小,同主族元素从上到下原子半径逐渐增大判断;
D.元素的非金属性越强,对应的氢化物越稳定.
解答:
解:A.非金属性Si<P<S<Cl,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,故A正确;
B.金属性Ca>Mg>Al,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,故B正确;
C.同主族元素从上到下原子半径逐渐增大,则O<S,同周期元素从左到右原子半径逐渐减小,则F<O、S<Na,故C正确;
D.非金属性F>O>S,元素的非金属性越强,对应的氢化物越稳定,应为HF>H2O>H2S,故D错误.
故选D.
B.金属性Ca>Mg>Al,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,故B正确;
C.同主族元素从上到下原子半径逐渐增大,则O<S,同周期元素从左到右原子半径逐渐减小,则F<O、S<Na,故C正确;
D.非金属性F>O>S,元素的非金属性越强,对应的氢化物越稳定,应为HF>H2O>H2S,故D错误.
故选D.
点评:本题综合考查元素周期律知识,为高考常见题型,侧重于学生的分析能力和综合运用化学知识的能力的考查,注意把握元素周期律的递变规律以及元素的金属性、非金属性与对应单质、化合物的关系,难度不大.

练习册系列答案
相关题目
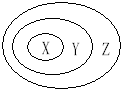 下列各选项中,各类物质依次表示为X、Y、Z,其中与如图三个圆所示的从属关系不相符的是( )
下列各选项中,各类物质依次表示为X、Y、Z,其中与如图三个圆所示的从属关系不相符的是( )| A、置换反应、氧化还原反应、化学反应 |
| B、胶体、溶液、混合物 |
| C、NaOH、电解质、化合物 |
| D、Fe2O3、金属氧化物、氧化物 |
下列物质分子中的氢原子不在同一平面上的有( )
| A、C2H2 |
| B、C2H4 |
| C、C2H6 |
| D、C6H6 |
 某有机物A的结构简式如图所示,某同学对其可能具有的化学性质进行了如下预测
某有机物A的结构简式如图所示,某同学对其可能具有的化学性质进行了如下预测①可以使酸性高锰酸钾溶液褪色
②可以和NaOH溶液反应
③在一定条件下可以和乙酸发生反应
④在一定条件下可以发生消去反应
⑤在一定条件下可以和新制Cu(OH)2反应
⑥遇FeCl3溶液可以发生显色反应.其中正确的是( )
| A、①②③⑥ | B、①②③⑤ |
| C、①②③④ | D、①②④⑤ |
下列关于有机物的说法错误的是( )
| A、CCl4可由CH4制得,可萃取碘水中的碘 |
| B、石油和天然气的主要成分都是碳氢化合物 |
| C、苯不能使KMnO4溶液褪色,因此苯不能发生氧化反应 |
| D、乙醇、乙酸和乙酸乙酯能用饱和Na2CO3溶液鉴别 |
下列说法正确的为( )
| A、含有共价键的化合物称为共价化合物 |
| B、共价化合物里只存在共价键 |
| C、离子化合物里只存在离子键 |
| D、离子化合物只含有离子键的化合物 |
下列物质中,能够导电,但不属于电解质的是( )
| A、NaOH固体 | B、稀盐酸 |
| C、熔化的NaCl | D、蔗糖 |
在Ba(OH)2?8H2O与NH4Cl的吸热反应实验中,需要将它们的晶体在研钵中研细,其作用是( )
| A、提高反应限度 |
| B、降低反应限度 |
| C、增大反应速率 |
| D、减小反应速率 |