题目内容
8.科学家将水置于一个足够强的电场中,在20℃时,水分子瞬间凝固形成“暖冰”.下列关于“暖冰”的说法正确的是( )| A. | “暖冰”中的水分子存在π键 | |
| B. | 水变成“暖冰”,体积会变小 | |
| C. | 在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰” | |
| D. | -个水分子与其他水分子间只能形成2个氢键 |
分析 A、“暖冰”中的水分子中氧原子含有2个σ键和2个孤对电子;
B、暖冰中氢键比水中多;
C、根据题意知,电场作用下,水分子间更易制得“暖冰”;
D、每个水分子与相邻四个水分子形成四个氢键.
解答 解:A、“暖冰”中的水分子中氧原子含有2个σ键和2个孤对电子,所以不存在π键,故A错误;
B、由于暖冰中氢键比水中多,所以水变成“暖冰”,体积会变大,故B错误;
C、在电场作用下,水分子间更易形成氢键,因而可以制得“暖冰”,否则20℃时,水分子不能瞬间凝固形成冰,故C正确;
D、水分子中氧原子含有一对孤对电子,O原子电负性较大,可以和其它的水分子形成两个氢键,含有的两个氢原子,可以分别和其它的水分子的氧原子形成两个氢键,所以以一个水分子为中心的正四面体结构,每个水分子与相邻四个水分子形成四个氢键,故D错误;
故选C.
点评 本题考查了水分子的间作用力及其影响因素等知识点,题目难度不大,注意水分子之间存在氢键,暖冰主要通过氢键形成固体.

练习册系列答案
相关题目
16.ClO2是一种杀菌消毒效率高、二次污染小的水处理剂.实验室中可通过以下反应制得:2KClO3+H2C2O4+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$2ClO2↑+K2SO4+2CO2+2H2O↑.下列有关该反应的说法正确的是( )
| A. | H2C2O4是氧化剂 | |
| B. | KClO3是还原剂 | |
| C. | H2C2O4在反应中被氧化 | |
| D. | 1molKClO3参加反应有2mol电子转移 |
3.化学与社会、生产、生活密切相关.下列说法错误的是( )
| A. | 地沟油经过加工处理后,可以用来制肥皂和生物柴油 | |
| B. | PM2.5颗粒(微粒直径约为2.5×10-6m)分散在空气中形成气溶胶 | |
| C. | 采用纳米TiO2光触媒技术,可将装修材料中释放的HCHO转化为无害物质 | |
| D. | 神舟十一号飞船所用太阳能电池板可将光能转换为电能,所用转换材料是硅晶体 |
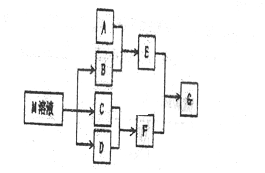
20.NiCl2是化工合成中最重要的镍源,工业上以金属镍废料(含Fe、Ca、Mg等杂质)为原料生产NiCl2,继而生产Ni2O3的工艺流程如图:

已知:1.Ksp( CaF2)=1.5×10-10Ksp(MgF2)=7.4×10-11Ksp(NiCO3)=1.42×10-7
2.流程中相关金属离子生成氢氧化物沉淀的pH如表所示:
(1)为了提高镍元素的浸出率,在“酸浸”时可采取的措施有:增大盐酸的浓度(或将镍废料研成粉末或延长浸泡时间等)(写出一种即可).
(2)加入H2O2时发生主要反应的离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O.
(3)“除铁”时,控制溶液pH的范围为3.2~7.1.
(4)滤渣B的主要成分的化学式为MgF2、CaF2.
(5)确保沉镍完全(即溶液中c(Ni2+)<1.0×10-6),保持溶液中c(CO32-)>0.142mol•L-1.
(6)“氧化”生成Ni2O3的离子方程式为2Ni2++ClO-+4OH-=Ni2O3↓+Cl-+2H2O.

已知:1.Ksp( CaF2)=1.5×10-10Ksp(MgF2)=7.4×10-11Ksp(NiCO3)=1.42×10-7
2.流程中相关金属离子生成氢氧化物沉淀的pH如表所示:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.1 | 6.5 | 7.1 |
| 沉淀完全的pH | 3.2 | 9.7 | 9.2 |
(2)加入H2O2时发生主要反应的离子方程式为2Fe2++H2O2+2H+═2Fe3++2H2O.
(3)“除铁”时,控制溶液pH的范围为3.2~7.1.
(4)滤渣B的主要成分的化学式为MgF2、CaF2.
(5)确保沉镍完全(即溶液中c(Ni2+)<1.0×10-6),保持溶液中c(CO32-)>0.142mol•L-1.
(6)“氧化”生成Ni2O3的离子方程式为2Ni2++ClO-+4OH-=Ni2O3↓+Cl-+2H2O.
12.下列有关实验原理或实验操作正确的是( )
| A. | 利用丁达尔效应鉴别FeCl3溶液和Fe(OH)3胶体 | |
| B. | 只能利用焰色反应可鉴别KCl溶液和Na2SO4溶液 | |
| C. | 用水润湿pH试纸测量某溶液的PH | |
| D. | 实验室用NaOH溶液除去Cl2中的少量HCl |
 3-甲基戊烷
3-甲基戊烷 2,2-二甲基-3-乙基戊烷.
2,2-二甲基-3-乙基戊烷.