题目内容
9.下列离子方程式的书写正确的是( )| A. | 玻璃试剂瓶被烧碱溶液腐蚀:SiO2+2Na++2OH-═Na2SiO3↓+H2O | |
| B. | 向NaHCO3溶液中加入少量的澄清石灰水,出现白色沉淀:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- | |
| C. | 硝酸铝溶液中加入过量氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | NaHSO3溶液中投入过氧化钠粉末:4HSO3-+2Na2O2═4SO32-+O2↑+4Na++2H2O |
分析 A.钠离子实际不参加反应,硅酸钠不是沉淀;
B.反应生成碳酸钠、碳酸钙和水;
C.反应生成氢氧化铝和硝酸铵;
D.发生氧化还原反应生成硫酸钠.
解答 解:A.玻璃试剂瓶被烧碱溶液腐蚀的离子反应为SiO2+2OH-═SiO32-+H2O,故A错误;
B.向NaHCO3溶液中加入少量的澄清石灰水,出现白色沉淀的离子反应为Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32-,故B正确;
C.硝酸铝溶液中加入过量氨水的离子反应为Al3++3NH3•H2O═Al(OH)3↓+3NH4+,故C错误;
D.NaHSO3溶液中投入过氧化钠粉末的离子反应为2H2O+HSO3-+3Na2O2═SO42-+O2↑+6Na++5OH-,故D错误;
故选B.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,注意离子反应中保留化学式的物质及电子、电荷守恒,选项D为解答的难点,题目难度不大.

练习册系列答案
 孟建平错题本系列答案
孟建平错题本系列答案 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目
3.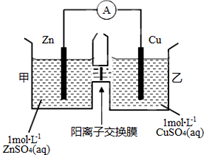 锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过.下列有关叙述不正确的是( )
锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过.下列有关叙述不正确的是( )
 锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过.下列有关叙述不正确的是( )
锌铜原电池装置如图所示,其中阳离子交换膜只允许阳离子和水分子通过.下列有关叙述不正确的是( )| A. | Zn电极上发生氧化反应 | |
| B. | 电子的流向为Zn→电流表→Cu | |
| C. | SO42-由乙池通过离子交换膜向甲池移动 | |
| D. | 电池工作一段时间后,乙池溶液的总质量明显增加 |
4.X、Y、Z是短周期三种元素,它们在周期表中的位置如图所示.试回答:
(1)X元素单质的化学式是He.
(2)Z元素的原子结构示意图为 .
.
(3)Y在元素周期表中的位置是第二周期、ⅤⅡA族.
(4)与Z同主族的下一周期元素的原子序数是34.
| X | ||
| Y | ||
| Z |
(2)Z元素的原子结构示意图为
 .
.(3)Y在元素周期表中的位置是第二周期、ⅤⅡA族.
(4)与Z同主族的下一周期元素的原子序数是34.
1.把锌片投人到盛有CH3COOH溶液的敞口容器里,改变下列条件,其中能加快反应速率的是( )
| A. | 加入少量NaCl固体 | B. | 滴加少量硫酸铜溶液 | ||
| C. | 加入少量水 | D. | 加入少量CH3COONa固体 |
14.下列反应的离子方程式正确的是( )
| A. | 乙醛溶液与新制氢氧化铜悬浊液共热CH3CHO+2Cu(OH)2+OH-$\stackrel{△}{→}$CH3COO-+Cu2O↓+2H2O | |
| B. | 甲酸溶液与新制氢氧化铜反应:2H++Cu(OH)2→Cu2++2H2O | |
| C. | 苯酚钠溶液中通入少量二氧化碳: +CO2+H2O$\stackrel{△}{→}$ +CO2+H2O$\stackrel{△}{→}$ +HCO3- +HCO3- | |
| D. | 乙酸乙酯与氢氧化钠溶液反应:CH3COOCH2CH3+OH-→CH3COO-+CH3CH2O-+H2O |
18.相同条件下,相同质量的乙烯和CO具有相同的( )
①分子数②体积③密度④原子数.
①分子数②体积③密度④原子数.
| A. | ①② | B. | ①②③ | C. | ①②③④ | D. | 以上都不相同 |
 .
. .
.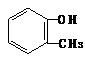 .
.
 ;
;