题目内容
部分弱酸的电离平衡常数如下表:
下列选项错误的是( )
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数 (25℃) |
Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A、2CN-+H2O+CO2→2HCN+CO32- |
| B、2HCOOH+CO32-→2HCOO-+H2O+CO2↑ |
| C、中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者 |
| D、等体积、等浓度的HCOONa和NaCN溶液中所含离子总数前者大于后者 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:弱酸的电离平衡常数越大,其酸性越强,等pH的弱酸溶液,酸性越强的酸其物质的量浓度越小,弱酸根离子水解程度越小,结合强酸能和弱酸盐反应制取弱酸分析解答.
解答:
解:酸的电离平衡常数HCOOH>H2CO3>HCN>HCO3-,则酸根离子水解程度CO32->CN->HCO3->HCOO-,
A.酸的电离平衡常数越大,酸的酸性越强,强酸能够制取弱酸,所以二者反应生成HCN和HCO3-,离子方程式为CN-+H2O+CO2═HCN+HCO3-,故A错误;
B.酸性强弱顺序是HCOOH>H2CO3>HCN>HCO3-,强酸能和弱酸盐反应生成弱酸,所以反应方程式为2HCOOH+CO32-=2HCOO-+H2O+CO2↑,故B正确;
C.等pH、等体积的HCOOH和HCN,n(HCN)>n(HCOOH),中和酸需要碱的物质的量与酸的物质的量、酸的元数成正比,所以中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者,故C正确;
D.根据电荷守恒,c(HCOO-)+c(OH-)=c(Na+)+c(H+),c(CN-)+c(OH-)=c(Na+)+c(H+),即离子总数是n(Na+ )+n(H+)的2倍,而NaCN的水解程度大,即NaCN溶液中的c(OH-)大,c(H+)小,c(Na+)相同,所以甲酸钠中离子浓度大,故D正确.
故选A.
A.酸的电离平衡常数越大,酸的酸性越强,强酸能够制取弱酸,所以二者反应生成HCN和HCO3-,离子方程式为CN-+H2O+CO2═HCN+HCO3-,故A错误;
B.酸性强弱顺序是HCOOH>H2CO3>HCN>HCO3-,强酸能和弱酸盐反应生成弱酸,所以反应方程式为2HCOOH+CO32-=2HCOO-+H2O+CO2↑,故B正确;
C.等pH、等体积的HCOOH和HCN,n(HCN)>n(HCOOH),中和酸需要碱的物质的量与酸的物质的量、酸的元数成正比,所以中和等体积、等pH的HCOOH和HCN消耗NaOH的量前者小于后者,故C正确;
D.根据电荷守恒,c(HCOO-)+c(OH-)=c(Na+)+c(H+),c(CN-)+c(OH-)=c(Na+)+c(H+),即离子总数是n(Na+ )+n(H+)的2倍,而NaCN的水解程度大,即NaCN溶液中的c(OH-)大,c(H+)小,c(Na+)相同,所以甲酸钠中离子浓度大,故D正确.
故选A.
点评:本题考查了弱电解质的电离,明确弱电解质电离平衡常数与酸性强弱、酸根离子的水解程度的关系是解本题关系,再结合强酸制取弱酸、酸碱中和反应来分析解答,易错选项是D,注意从电荷守恒的角度解答该题.

练习册系列答案
相关题目
下列气体有毒的是( )
| A、N2 |
| B、H2 |
| C、O2 |
| D、Cl2 |
下列物质中,肯定能发生化学反应而使溴的CCl4溶液和酸性高锰酸钾溶液褪色的( )
| A、甲苯 |
| B、C3H6 |
| C、C5H12 |
| D、C2H4 |
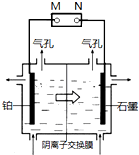 制备单质锰的实验装置如图,阳极以稀硫酸为电解液,阴极以硫酸锰和硫酸混合液为电解液,电解装置中箭头表示溶液中阴离子移动的方向.下列说法不正确的是( )
制备单质锰的实验装置如图,阳极以稀硫酸为电解液,阴极以硫酸锰和硫酸混合液为电解液,电解装置中箭头表示溶液中阴离子移动的方向.下列说法不正确的是( )| A、M是电源的负极 | ||||
| B、左侧气孔逸出的气体可能为副产物H2 | ||||
C、电解槽中发生的总反应为:MnSO4+2H2O
| ||||
| D、若用阳离子交换膜代替阴离子交换膜,阳极可能得到 MnO2 |
设NA代表阿伏加德罗常数(NA)的数值,下列说法正确的是( )
| A、1mol硫酸钾中阴离子所带电荷数为NA | ||
| B、18g水中含有的电子数为10NA | ||
C、标准状况下,1L水所含分子数为
| ||
| D、将含0.1mol氯化铁的饱和溶液滴加到沸水中可制取0.1NA个Fe(OH)3胶体微粒 |
下列离子方程式正确的是( )
| A、铁和盐酸反应:2Fe+6H+=2Fe3++3H2↑ |
| B、氯化铁和铜反应:Fe3++Cu=Fe2++Cu2+ |
| C、澄清石灰水与碳酸钠溶液混合:Ca(OH)2+CO32-=CaCO3↓+2OH- |
| D、用醋酸除水垢:2CH3COOH+CaCO3=2CH3COO-+Ca2++H2O+CO2↑ |
 如图,在盛有H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )
如图,在盛有H2SO4的烧杯中放入用导线连接的电极X、Y,外电路中电子流向如图所示,关于该装置的下列说法正确的是( )| A、外电路的电流方向为:X→外电路→Y |
| B、若两电极分别为Fe和碳棒,则X为碳棒,Y为Fe |
| C、X极上发生的是还原反应,Y极上发生的是氧化反应 |
| D、溶液中氢离子向Y极移动,硫酸根向X极移动 |
乙烷跟氯气在光照下发生取代反应,得到乙烷的氯代产物最多有( )
| A、10种 | B、9种 | C、8种 | D、7种 |