题目内容
ClO2作为一种广谱型的消毒剂,将逐渐用来取代Cl2成为自来水的消毒剂.已知ClO2是一种易溶于水而难溶于有机溶剂的气体,实验室制备ClO2的原理是用亚氯酸钠固体与纯净的氯气反应 2NaClO2+Cl2═2ClO2+2NaCl
如图1是实验室用于制备和收集一定量纯净的ClO2的装置(某些夹持装置和垫持用品省略).其中E中盛有CCl4液体.

(1)仪器P的名称是
(2)写出装置A中烧瓶内发生反应的化学方程式:
(3)E装置中所盛试剂的作用是
(4)F处应选用的收集装置是图2 (填序号),其中与E装置导管相连的导管口是图2 (填接口字母).

(5)以下是尾气吸收装置,能用于吸收多余ClO2气体,并能防止倒吸的装置的是如图3的

A.①②B.②③C.③④D.②④
(6)若用100mL 2mol?L-1的浓盐酸与足量的MnO2制备Cl2,则被氧化的HCl的物质的量是 (填序号).
A.>0.1mol B.0.1mol C.<0.1mol D.无法判断.
(7)ClO2也可由KClO3在H2SO4溶液存在下与Na2SO3反应制得.请写出反应的离子方程式: .
如图1是实验室用于制备和收集一定量纯净的ClO2的装置(某些夹持装置和垫持用品省略).其中E中盛有CCl4液体.

(1)仪器P的名称是
(2)写出装置A中烧瓶内发生反应的化学方程式:
(3)E装置中所盛试剂的作用是
(4)F处应选用的收集装置是图2

(5)以下是尾气吸收装置,能用于吸收多余ClO2气体,并能防止倒吸的装置的是如图3的

A.①②B.②③C.③④D.②④
(6)若用100mL 2mol?L-1的浓盐酸与足量的MnO2制备Cl2,则被氧化的HCl的物质的量是
A.>0.1mol B.0.1mol C.<0.1mol D.无法判断.
(7)ClO2也可由KClO3在H2SO4溶液存在下与Na2SO3反应制得.请写出反应的离子方程式:
考点:氯、溴、碘及其化合物的综合应用
专题:卤族元素
分析:由题目中所给信息和实验装置图可知:本实验首先用浓盐酸和MnO2在加热条件下反应制备Cl2,反应的方程式为MnO2+4HCl
MnCl2+Cl2↑+2H2O,经除杂、干燥后在D中亚氯酸钠固体反应生成ClO2,由于Cl2易溶于CCl4液体,E用于除去ClO2中的未反应的Cl2,最后用向上排空法收集;并注意气体的性质和装置来分析防止倒吸的装置,利用稀盐酸与二氧化锰不反应来分析浓盐酸与足量的MnO2制备Cl2,则被氧化的HCl的物质的量.
(1)实验室用浓盐酸和MnO2在加热条件下反应制备Cl2,浓盐酸应盛装在分液漏斗中,则P为分液漏斗;
(2)浓盐酸和MnO2在加热条件下反应制备Cl2;
(3)生成的ClO2中混有氯气,为制备纯净干燥的ClO2,根据氯气易溶于四氯化碳的也远了,使用四氯化碳来除去氯气;
(4)ClO2是一种易溶于水的气体,且密度比空气大,应用向上排空气法收集,且进行尾气处理,故用双孔橡皮塞;
(5)ClO2是一种易溶于水的气体,尾气吸收时要防止倒吸,导气管不能插入到液面以下;
(6)浓盐酸在加热条件下与二氧化锰发生氧化还原反应,但随着反应的进行,盐酸浓度变稀时,不与二氧化锰反应;
(7)由KClO3在H2SO4存在下与Na2SO3反应制得二氧化氯,还生成硫酸钾、水.
| ||
(1)实验室用浓盐酸和MnO2在加热条件下反应制备Cl2,浓盐酸应盛装在分液漏斗中,则P为分液漏斗;
(2)浓盐酸和MnO2在加热条件下反应制备Cl2;
(3)生成的ClO2中混有氯气,为制备纯净干燥的ClO2,根据氯气易溶于四氯化碳的也远了,使用四氯化碳来除去氯气;
(4)ClO2是一种易溶于水的气体,且密度比空气大,应用向上排空气法收集,且进行尾气处理,故用双孔橡皮塞;
(5)ClO2是一种易溶于水的气体,尾气吸收时要防止倒吸,导气管不能插入到液面以下;
(6)浓盐酸在加热条件下与二氧化锰发生氧化还原反应,但随着反应的进行,盐酸浓度变稀时,不与二氧化锰反应;
(7)由KClO3在H2SO4存在下与Na2SO3反应制得二氧化氯,还生成硫酸钾、水.
解答:
解:(1)实验室用浓盐酸和MnO2在加热条件下反应制备Cl2,浓盐酸应盛装在分液漏斗中,则P为分液漏斗;
故答案为:分液漏斗;
(2)浓盐酸和MnO2在加热条件下反应制备Cl2,反应的方程式为MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
故答案为:MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O;
(3)生成的ClO2中混有氯气,为制备纯净干燥的ClO2,根据氯气易溶于四氯化碳的也远了,使用四氯化碳来除去氯气;
故答案为:用于除去ClO2中未反应的Cl2;
(4)ClO2是一种易溶于水的气体,且密度比空气大,应用向上排空气法收集,且进行尾气处理,故用双孔橡皮塞;
故答案为:②;d;
(5)ClO2是一种易溶于水的气体,尾气吸收时要防止倒吸,导气管不能插入到液面以下,②④符合;
故答案为:D;
(6)浓盐酸在加热条件下与二氧化锰发生氧化还原反应,但随着反应的进行,盐酸浓度变稀时,不与二氧化锰反应,根据MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O可知,若用100mL 2mol?L-1的浓盐酸与足量的MnO2制备Cl2,则被氧化的HCl的物质的量<0.1mol;
故答案为:C;
(7)KClO3在H2SO4存在下与Na2SO3反应,SO32-被氧化成SO42-,由电子、电荷守恒可知该离子反应为2ClO3-+SO32-+2H+═2ClO2+SO42-+H2O,
故答案为:2ClO3-+SO32-+2H+═2ClO2+SO42-+H2O.
故答案为:分液漏斗;
(2)浓盐酸和MnO2在加热条件下反应制备Cl2,反应的方程式为MnO2+4HCl(浓)
| ||
故答案为:MnO2+4HCl(浓)
| ||
(3)生成的ClO2中混有氯气,为制备纯净干燥的ClO2,根据氯气易溶于四氯化碳的也远了,使用四氯化碳来除去氯气;
故答案为:用于除去ClO2中未反应的Cl2;
(4)ClO2是一种易溶于水的气体,且密度比空气大,应用向上排空气法收集,且进行尾气处理,故用双孔橡皮塞;
故答案为:②;d;
(5)ClO2是一种易溶于水的气体,尾气吸收时要防止倒吸,导气管不能插入到液面以下,②④符合;
故答案为:D;
(6)浓盐酸在加热条件下与二氧化锰发生氧化还原反应,但随着反应的进行,盐酸浓度变稀时,不与二氧化锰反应,根据MnO2+4HCl(浓)
| ||
故答案为:C;
(7)KClO3在H2SO4存在下与Na2SO3反应,SO32-被氧化成SO42-,由电子、电荷守恒可知该离子反应为2ClO3-+SO32-+2H+═2ClO2+SO42-+H2O,
故答案为:2ClO3-+SO32-+2H+═2ClO2+SO42-+H2O.
点评:本题考查气体的制备、除杂、收集等实验操作,题目难度不大,学习中注意把握化学实验基本操作,做该类题目时把握实验目的和实验原理是解答题目的关键.

练习册系列答案
相关题目
下列物质含分子最多的是( )
| A、1.204×1024个O2 |
| B、3molCO2 |
| C、标准状况下89.6LCl2 |
| D、标准状况下90mL水(水的密度为1g/mL) |
下列各对物质,互为同系物的是:( )
A、H3C-CH=CH2与 |
B、 与 与 |
| C、HCOOCH3与CH3COOH |
D、 与 与 |
下列既能与Na、NaOH、Na2CO3反应,又能与乙醇反应的是( )
| A、酒精 | B、乙酸 | C、甲烷 | D、苯 |
对于常温下pH为12的氢氧化钠溶液,叙述正确的是( )
| A、将此溶液稀释106倍,溶液的pH=6 |
| B、与等体积等浓度的氯化铵溶液混合后所得溶液呈中性 |
| C、与pH=2的CH3COOH溶液任意比混合:c(H+)+c(Na+)=c(OH-)+c(CH3COO-) |
| D、与0.01 mol?L-1 的CH3COOH溶液等体积混合所得溶液中:c (Na+)>c(CH3COO-)>c(OH-)>c(H+) |
下列关于强、弱电解质的叙述,有错误的是( )
| A、电解质本身不一定能导电 |
| B、在溶液中,导电能力弱的电解质不一定是弱电解质 |
| C、纯净的强电解质在液态时,有的导电,有的不导电 |
| D、SO2的水溶液能导电,所以SO2是电解质 |
下列图示与对应的叙述相符的是( )
A、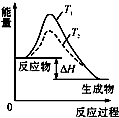 温度T1>T2,SO2与O2反应过程中的能量变化 |
B、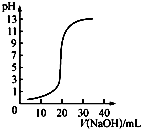 表示0.100 0 mol/L NaOH溶液滴定20.00 mL 0.100 0 mol/L CH3COOH溶液 |
C、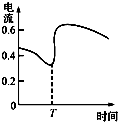 表示Zn、Cu和稀硫酸构成的原电池中电流强度的变化,T时加入了H2O2 |
D、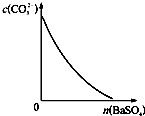 表示在饱和Na2CO3溶液中逐步加BaSO4固体后,溶液中c(CO32-)的浓度变化 |
 1L某混合溶液中,溶质X、Y的浓度都为0.1mol/L,向混合溶液中滴加某溶液Z(0.1mol/L的氢氧化钠或硫酸溶液),所得沉淀的物质的量随着Z溶液的体积变化关系如图所示,则X、Y、Z分别是( )
1L某混合溶液中,溶质X、Y的浓度都为0.1mol/L,向混合溶液中滴加某溶液Z(0.1mol/L的氢氧化钠或硫酸溶液),所得沉淀的物质的量随着Z溶液的体积变化关系如图所示,则X、Y、Z分别是( )| A、AlCl3、FeCl3、NaOH |
| B、AlCl3、MgCl2、NaOH |
| C、NaAlO2、Ba(OH)2、H2SO4 |
| D、NaAlO2、BaCl2、H2SO4 |