题目内容
Al、Fe、Cu都是重要的金属元素,下列说法正确的是
A.三者对应的氧化物均为碱性氧化物
B.三者的单质放置在空气中均只生成氧化物
C.制 备AlCl3、FeCl3、CuCl2固体均不能采用将溶液
备AlCl3、FeCl3、CuCl2固体均不能采用将溶液 直接蒸干的方法
直接蒸干的方法
D.电解AlCl3、FeCl3、CuCl2 的混合溶液时阴极上依次析出Cu、Fe、Al
的混合溶液时阴极上依次析出Cu、Fe、Al
C
【解析】
试题分析:A、Al对应的氧化物是氧化铝,而氧化铝属于两性氧化物,错误;B、Cu的单质放在空气中,可生成铜绿碱式碳酸铜,属于盐,错误;C、水解的氯化物中,因为生成生成难溶碱和HCl,加热促进水解,同时HCl的挥发,也使水解正向移动,所以最终得到是难溶碱,不会得到氯化物固体,所以制 备AlCl3、FeCl3、CuCl2固体均不能采用将溶液
备AlCl3、FeCl3、CuCl2固体均不能采用将溶液 直接蒸干的方法,正确;D、因为阳离子的氧化性Fe3+>Cu2+>Fe2+>>H+>Al3+,所以电解AlCl3、FeCl3、CuCl2
直接蒸干的方法,正确;D、因为阳离子的氧化性Fe3+>Cu2+>Fe2+>>H+>Al3+,所以电解AlCl3、FeCl3、CuCl2 的混合溶液时,先是铁离子得到电子生成亚铁离子,其次是铜离子得到电子生成单质Cu,然后析出Fe,亚铁离子放电完全后,则是氢离子放电生成氢气,所以阴极上依次析出Cu、Fe、H2,错误,答案选C。
的混合溶液时,先是铁离子得到电子生成亚铁离子,其次是铜离子得到电子生成单质Cu,然后析出Fe,亚铁离子放电完全后,则是氢离子放电生成氢气,所以阴极上依次析出Cu、Fe、H2,错误,答案选C。
考点:考查氧化物的类型的判断,盐水解产物的判断,电解产物的判断

 阅读快车系列答案
阅读快车系列答案(12分)A、B、C、D为原子序数依次增大的四种短周期元素,其性质或结构信息如下表:
元素 | A | B | C | D | E |
性质 或结 构信 息 | 室温下单质呈气态,原子最外层电子数与D相同 | D3B中阳离子与阴离子的电子层结构相同 | A和C可形成两种常见的化合物甲和乙,乙具有弱酸性 | 单质质软、银白色固体、导电性强,在空气中燃烧生成淡黄色固体 | E的气态氢化物和最高价氧化物对应的水化物均为强酸,C、D和E三种元素形成的一种盐丙为某消毒液的主要成分 |
试回答以下问题
(1)B在周期表中的位置是 ,B的氢化物与E的氢化物比较,沸点较高的是 (填化学式)。
(2)D3B可与水反应生成2种碱性物质,请写出这一化学方程式 。
(3)写出丙的电子式为 。并说明丙在空气中漂白的原理(用化学方程式表示) 。(请参考下表数据)
酸 | 电离常数 |
HClO | Ka=3.0×10-8 |
H2CO3 | Ka1=4.3×10-7,Ka2=5.6×10-11 |
(4)由A、B、C、D四种元素中的三种元素组成的一种盐丁,其外观与氯化钠相似,丁的水溶液呈碱性。将光亮的铜丝插入丁溶液中,没有现象发生,如用盐酸酸化,反应迅速发生,铜丝缓慢溶解生成深绿色溶液,写出该反应的离子方程式 。
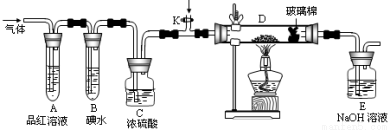
 A中观察到的现象是否相同 (填“相同”或“不相同”);若装置D中装的是铁粉,当通入足量W2时观察到的现象为 ;若装置D中装的是五氧化二钒(作催化剂),当通入足量YX2时,打开K通入适量X2,化学反应方程式为 ;
A中观察到的现象是否相同 (填“相同”或“不相同”);若装置D中装的是铁粉,当通入足量W2时观察到的现象为 ;若装置D中装的是五氧化二钒(作催化剂),当通入足量YX2时,打开K通入适量X2,化学反应方程式为 ; 。
。 原子半径最大,元素D的
原子半径最大,元素D的 合金是日常生活中常用的金属材料。下列说法正确的是
合金是日常生活中常用的金属材料。下列说法正确的是