题目内容
某兴趣小组在研究性学习中设计了如下实验探究Fe和H2SO4反应的过程,装置如图所示.
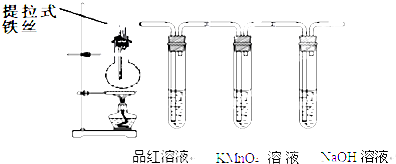
①在烧瓶中加入浓硫酸.
②将提拉式铁丝插入溶液中,观察到有少量气泡,后停止的现象.
③加热烧瓶至有大量气体 产生时停止加热,品红溶液颜色褪去,烧瓶中溶液变为棕黄色.
④一段时间后KMnO4溶液颜色不再变浅,但NaOH 溶液中仍有气体放出,在导管口处可点燃此气体,烧瓶中液体变为浅绿色
根据以上实验回答:
(1)由步骤②的现象可得出的结论是:
(2)在步骤③中,品红溶液褪色的原因是
(3)写出步骤④中,使溶液变为浅绿色的可能的原因是(用离子方程式表示) ;
(4)KMnO4溶液褪色的化学方程式 .
(5)设计实验证明反应后的溶液中只有Fe2+(答操作和现象)
(6)若在反应中铁丝质量减少a克,并收集到bL可燃性气体(标准状况下假设无体积损失),则在反应过程中产生的使品红溶液褪色的气体的质量是 (用含a、b数学表达式表示)

①在烧瓶中加入浓硫酸.
②将提拉式铁丝插入溶液中,观察到有少量气泡,后停止的现象.
③加热烧瓶至有大量气体 产生时停止加热,品红溶液颜色褪去,烧瓶中溶液变为棕黄色.
④一段时间后KMnO4溶液颜色不再变浅,但NaOH 溶液中仍有气体放出,在导管口处可点燃此气体,烧瓶中液体变为浅绿色
根据以上实验回答:
(1)由步骤②的现象可得出的结论是:
(2)在步骤③中,品红溶液褪色的原因是
(3)写出步骤④中,使溶液变为浅绿色的可能的原因是(用离子方程式表示)
(4)KMnO4溶液褪色的化学方程式
(5)设计实验证明反应后的溶液中只有Fe2+(答操作和现象)
(6)若在反应中铁丝质量减少a克,并收集到bL可燃性气体(标准状况下假设无体积损失),则在反应过程中产生的使品红溶液褪色的气体的质量是
考点:性质实验方案的设计
专题:
分析:(1)在常温下铁在浓硫酸中发生钝化;
(2)根据二氧化硫具有漂白性的知识来回答;
(3)金属铁可以和稀硫酸反应还可以和三价铁反应;
(4)二氧化硫与高锰酸钾发生氧化还原反应生成锰离子和硫酸根;
(5)溶液中加硫氰化钾溶液,不变红色,说明没有三价铁离子,再加氯气变红色说明含有亚铁离子;
(6)收集到bL可燃性气体为氢气,则可以求出生成氢气消耗的Fe,再结合得失电子守恒计算.
(2)根据二氧化硫具有漂白性的知识来回答;
(3)金属铁可以和稀硫酸反应还可以和三价铁反应;
(4)二氧化硫与高锰酸钾发生氧化还原反应生成锰离子和硫酸根;
(5)溶液中加硫氰化钾溶液,不变红色,说明没有三价铁离子,再加氯气变红色说明含有亚铁离子;
(6)收集到bL可燃性气体为氢气,则可以求出生成氢气消耗的Fe,再结合得失电子守恒计算.
解答:
解:(1)常温下将Fe丝插入硫酸中会有气泡产生,说明发生了反应,但一会儿后即停止,说明Fe在硫酸中发生了钝化,阻止了反应的进一步进行,
故答案为:在常温下铁在浓硫酸中发生钝化;
(2)Fe与浓H2SO4反应可能是浓H2SO4强氧化性或是发生置换反应生成H2,则实验现象品红溶液褪色说明产生的是SO2气体,
故答案为:生成的二氧化硫具有漂白性;
(3)溶液变为浅绿色说明产生了Fe2+,一种可能是Fe与H2SO4反应生成FeSO4,也存在Fe3+离子转化为Fe2+,故答案为:Fe+2 H+=Fe2++H2,Fe+2Fe3+=3Fe2+;
(4)二氧化硫与高锰酸钾发生氧化还原反应生成锰离子和硫酸根,其反应的化学方程式为:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4;
故答案为:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4;
(5)取适量反应后的溶液放入试管中,加入KSCN溶液无明显现象,再加入少量氯水,溶液变红则证明溶液中含有Fe2+但不含Fe3+;
故答案为:取适量反应后的溶液放入试管中,加入KSCN溶液无明显现象,再加入少量氯水,溶液变红则证明溶液中含有Fe2+但不含Fe3+;
(6)收集到bL可燃性气体氢气,根据化学方程式Fe+2H+=Fe2++H2可以知道消耗金属铁的物质的量为
mol,
则和三价铁反应消耗金属铁的物质的量为(
-
)mol,
由电子守恒可知该物质的量和生成二氧化硫的量相等,所以生成二氧化硫的质量为64(
-
)g,
故答案为:64(
-
).
故答案为:在常温下铁在浓硫酸中发生钝化;
(2)Fe与浓H2SO4反应可能是浓H2SO4强氧化性或是发生置换反应生成H2,则实验现象品红溶液褪色说明产生的是SO2气体,
故答案为:生成的二氧化硫具有漂白性;
(3)溶液变为浅绿色说明产生了Fe2+,一种可能是Fe与H2SO4反应生成FeSO4,也存在Fe3+离子转化为Fe2+,故答案为:Fe+2 H+=Fe2++H2,Fe+2Fe3+=3Fe2+;
(4)二氧化硫与高锰酸钾发生氧化还原反应生成锰离子和硫酸根,其反应的化学方程式为:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4;
故答案为:5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4;
(5)取适量反应后的溶液放入试管中,加入KSCN溶液无明显现象,再加入少量氯水,溶液变红则证明溶液中含有Fe2+但不含Fe3+;
故答案为:取适量反应后的溶液放入试管中,加入KSCN溶液无明显现象,再加入少量氯水,溶液变红则证明溶液中含有Fe2+但不含Fe3+;
(6)收集到bL可燃性气体氢气,根据化学方程式Fe+2H+=Fe2++H2可以知道消耗金属铁的物质的量为
| b |
| 22.4 |
则和三价铁反应消耗金属铁的物质的量为(
| a |
| 56 |
| b |
| 22.4 |
由电子守恒可知该物质的量和生成二氧化硫的量相等,所以生成二氧化硫的质量为64(
| a |
| 56 |
| b |
| 22.4 |
故答案为:64(
| a |
| 56 |
| b |
| 22.4 |
点评:本题考查了实验探究Fe和H2SO4反应的过程,题目难度中等,侧重于考查学生的实验操作和处理实验数据能力,明确反应原理和有关物质的性质是解题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
室温时将100mLH2S和O2的混合气体,点燃完全反应后恢复到原来状况,体积变为40mL.下列叙述中正确的是( )
| A、剩余40mL气体一定是O2 |
| B、剩余40mL气体是H2S或SO2 |
| C、混合气体中含H2S 40mL或80mL |
| D、剩余40mL气体是SO2和O2混合气体 |
下列说法不正确的是( )
| A、二氧化硅晶体是一种无色透明的固体,常用作光导纤维的材料 |
| B、臭氧是一种有特殊臭味、氧化性极强的淡蓝色气体,可用作餐具的消毒剂 |
| C、铝及其合金是电气、工业、家庭广泛使用的材料,是因为铝比铁更耐酸、碱的腐蚀 |
| D、人造纤维可利用竹子、棉花、麻类的纤维材料制成,而合成纤维是利用自然界的非纤维材料(如石油、煤)通过化学合成方法得到 |
香叶醇是合成玫瑰香油的主要原料,其结构简式如图: 下列有关香叶醇的叙述错误的是( )
下列有关香叶醇的叙述错误的是( )
 下列有关香叶醇的叙述错误的是( )
下列有关香叶醇的叙述错误的是( )| A、香叶醇的分子式为C10H19O |
| B、能使溴的四氯化碳溶液褪色 |
| C、能使酸性高锰酸钾溶液褪色 |
| D、能发生取代反应,也能发生1,4加成反应 |
有机物 是常用的降血脂药物之一.下列有关它的说法正确的是( )
是常用的降血脂药物之一.下列有关它的说法正确的是( )
 是常用的降血脂药物之一.下列有关它的说法正确的是( )
是常用的降血脂药物之一.下列有关它的说法正确的是( )A、它是 的同系物 的同系物 |
| B、它能发生加成、取代、消去等反应 |
| C、它可使酸性KMnO4溶液褪色,但不能与溴水反应使其褪色 |
| D、它苯环上的一氯代物有三种 |
铁铜合金中逐滴加入稀硝酸的过程中,下列离子方程式较难发生的是( )
| A、Fe+4H++NO3-→Fe3++NO↑+2H2O |
| B、3Fe+8H++2 NO3-→3Fe2++2NO↑+4H2O |
| C、3Cu+8H++2 NO3-→3Cu2++2NO↑+4H2O |
| D、3Fe2++4H++NO3-→3Fe3++NO↑+2H2O |
设NA表示阿伏加德罗常数,下列说法不正确的是( )
| A、在0.1mol氢氧化钠中,阴、阳离子的个数比为1:1 |
| B、标准状况下,如果11.2LO2含有n个氧分子,则NA为2n |
| C、22.4L氢气所含原子数目为2NA |
| D、标准状况下,18克的水物质的量为1mol |
 某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示.
某校化学兴趣小组探究SO2与FeCl3溶液的反应,所用装置如图所示.