题目内容
室温时将100mLH2S和O2的混合气体,点燃完全反应后恢复到原来状况,体积变为40mL.下列叙述中正确的是( )
| A、剩余40mL气体一定是O2 |
| B、剩余40mL气体是H2S或SO2 |
| C、混合气体中含H2S 40mL或80mL |
| D、剩余40mL气体是SO2和O2混合气体 |
考点:有关混合物反应的计算
专题:计算题
分析:H2S和O2的混合气体点燃,氧气不足发生反应①2H2S+O2═2S↓+2H2O,氧气足量发生反应②2H2S+3O2═2SO2+2H2O,据此讨论,若n(H2S):n(O2)>2:1,发生反应①,H2S有剩余;若n(H2S):n(O2)=2:1,发生反应①,没有气体;若n(H2S):n(O2)<2:3,发生反应②,氧气有剩余,气体为氧气、二氧化硫;若n(H2S):n(O2)=2:3,发生反应②,气体为二氧化硫;若2:3<n(H2S):n(O2)<2:1,发生反应①②,气体为二氧化硫,据此计算判断.
解答:
解:H2S和O2的混合气体点燃,氧气不足发生反应①2H2S+O2═2S↓+2H2O,氧气足量发生反应②2H2S+3O2═2SO2+2H2O.
若n(H2S):n(O2)>2:1,发生反应①,H2S有剩余,则:
2 H2S+O2═2 S↓+2 H2O 体积变化△V;
2 1 3
40ml 20ml 100ml-40ml=60ml
剩余气体H2S为40ml,原混合气体中H2S为80ml,O2为20ml,符合题意;
若n(H2S):n(O2)=2:1,发生反应①,没有气体,H2S为66.7ml,O2为33.3ml,不符合题意;
若n(H2S):n(O2)<2:3,发生反应②,氧气有剩余,则:
2 H2S+3 O2═2 SO2+2H2O 体积变化△V;
2 3 2 3
40ml 60mL 40ml 100ml-40ml=60ml
硫化氢与氧气体积之和为100mL,没有氧气剩余,不符合题意;
若n(H2S):n(O2)=2:3,发生反应②,最后气体为二氧化硫,体积为40ml,原混合气体中H2S为40ml,O2为60ml,符合题意;
由上述计算,可知不可能存在2:3<n(H2S):n(O2)<2:1情况,
故剩余气体可能是40mLH2S或者40mLSO2,对应的原混合气体为H2S为80ml,O2为20ml或者H2S为40ml,O2为60ml,
故选BC.
若n(H2S):n(O2)>2:1,发生反应①,H2S有剩余,则:
2 H2S+O2═2 S↓+2 H2O 体积变化△V;
2 1 3
40ml 20ml 100ml-40ml=60ml
剩余气体H2S为40ml,原混合气体中H2S为80ml,O2为20ml,符合题意;
若n(H2S):n(O2)=2:1,发生反应①,没有气体,H2S为66.7ml,O2为33.3ml,不符合题意;
若n(H2S):n(O2)<2:3,发生反应②,氧气有剩余,则:
2 H2S+3 O2═2 SO2+2H2O 体积变化△V;
2 3 2 3
40ml 60mL 40ml 100ml-40ml=60ml
硫化氢与氧气体积之和为100mL,没有氧气剩余,不符合题意;
若n(H2S):n(O2)=2:3,发生反应②,最后气体为二氧化硫,体积为40ml,原混合气体中H2S为40ml,O2为60ml,符合题意;
由上述计算,可知不可能存在2:3<n(H2S):n(O2)<2:1情况,
故剩余气体可能是40mLH2S或者40mLSO2,对应的原混合气体为H2S为80ml,O2为20ml或者H2S为40ml,O2为60ml,
故选BC.
点评:本题考查混合物计算、过量计算、讨论计算等,难度中等,清楚反应过程是解题关键,对应选择题利用验证法进行解答更简单.

练习册系列答案
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案
相关题目
现有25mL2mol?L-1的Na2CO3溶液和50mL 1mol?L-1的稀盐酸.
(1)将Na2CO3溶液逐滴滴入稀盐酸中;
(2)将稀盐酸逐滴滴入Na2CO3溶液中.
两操作的现象及结果(标准状况下)为( )
(1)将Na2CO3溶液逐滴滴入稀盐酸中;
(2)将稀盐酸逐滴滴入Na2CO3溶液中.
两操作的现象及结果(标准状况下)为( )
| A、现象相同,所得气体的体积相等 |
| B、现象相同,所得气体的体积不等 |
| C、现象不同,所得气体的体积相等 |
| D、现象不同,所得气体的体积不等 |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
| A、c(H+)<c(OH-)的溶液中,Na+、K+、SO42-、ClO- |
| B、能使酚酞变红的溶液中:Na+、Cu2+、CO32-、NO3- |
| C、0.1mol?L-1FeCl3溶液中:K+、NH4-、I-、SCN- |
| D、加入铝粉能产生氢气的溶液中:NH4+、Fe2+、NO3-、SO42- |
下列说法错误的是( )
| A、在日常生活中,化学腐蚀是造成钢铁腐蚀的主要原因 |
| B、人们常采用牺牲阳极保护法防止通讯电缆发生腐蚀 |
| C、在电镀槽中,镀件做阴极,阳极选用镀层金属 |
| D、用惰性电极电解某硫酸铜溶液一段时间后,要恢复溶液的成分和浓度,可向溶液中加入一定量的氧化铜 |
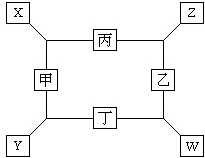 如图所示,已知:
如图所示,已知: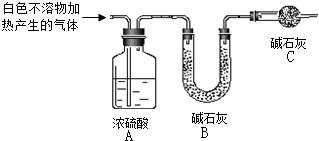 资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.某同学通过如下实验探究反应原理并验证产物.
资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物.某同学通过如下实验探究反应原理并验证产物.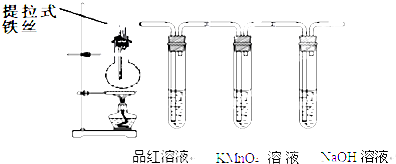
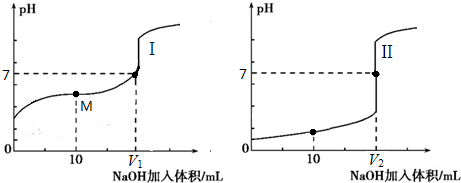 电解质的水溶液中存在电离平衡.
电解质的水溶液中存在电离平衡.