题目内容
 如图所示表示的是电解饱和食盐水的装置,阴极材料是铁棒,阳极材料是碳棒,饱和食盐水中含有少量酚酞.
如图所示表示的是电解饱和食盐水的装置,阴极材料是铁棒,阳极材料是碳棒,饱和食盐水中含有少量酚酞.(1)接通电源后,饱和食盐水中的阳离子的移动方向是
(2)电极上生成了气体A和B,生成气体A的电极反应式是
(3)随着气体的生成,饱和食盐水中产生了两种不同的颜色:一种是
(4)电解一段时间后取出电极,将U形管内的液体搅拌混匀,又发生了化学反应,该反应的化学方程式是
考点:电解原理
专题:
分析:(1)在电解池中,阳离子移向阴极;
(2)电解氯化钠溶液,在电解池的阴极上阳离子发生失电子的氧化反应,只会产生氢气,在阳极上发生失电子的还原反应,产生氯气;
(3)电解氯化钠溶液,阳极区产生氯气,阴极区显示碱性,碱遇到酚酞显示红色;
(4)氯气可以和氢氧化钠之间发生反应生成氯化钠、次氯酸钠和水.
(2)电解氯化钠溶液,在电解池的阴极上阳离子发生失电子的氧化反应,只会产生氢气,在阳极上发生失电子的还原反应,产生氯气;
(3)电解氯化钠溶液,阳极区产生氯气,阴极区显示碱性,碱遇到酚酞显示红色;
(4)氯气可以和氢氧化钠之间发生反应生成氯化钠、次氯酸钠和水.
解答:
解:(1)在电解池中,阳离子的移动方向是移向阴极,故答案为:阴极;
(2)电解氯化钠溶液,和正极相连的是阳极,该极上产生氯气,另一极是阴极,该极上产生氢气,2H++2e-=H2↑,故答案为:2H++2e-=H2↑;
(3)电解氯化钠溶液,氯离子在阳极区失电子产生氯气,氯气溶于水得到的氯水,显示浅黄绿色,阴极区是氢离子发生还原反应,产生氢气,该极区显示碱性,碱遇到酚酞显示红色,故答案为:浅黄绿色;阳极区;红;阴极区;
(4)氯气可以和氢氧化钠之间发生反应生成氯化钠、次氯酸钠和水,方程式为Cl2+2NaOH═NaCl+NaClO+H2O,次氯酸钠具有强氧化性,因而具有漂白性,
故答案为:Cl2+2NaOH═NaCl+NaClO+H2O;NaClO有强氧化性.
(2)电解氯化钠溶液,和正极相连的是阳极,该极上产生氯气,另一极是阴极,该极上产生氢气,2H++2e-=H2↑,故答案为:2H++2e-=H2↑;
(3)电解氯化钠溶液,氯离子在阳极区失电子产生氯气,氯气溶于水得到的氯水,显示浅黄绿色,阴极区是氢离子发生还原反应,产生氢气,该极区显示碱性,碱遇到酚酞显示红色,故答案为:浅黄绿色;阳极区;红;阴极区;
(4)氯气可以和氢氧化钠之间发生反应生成氯化钠、次氯酸钠和水,方程式为Cl2+2NaOH═NaCl+NaClO+H2O,次氯酸钠具有强氧化性,因而具有漂白性,
故答案为:Cl2+2NaOH═NaCl+NaClO+H2O;NaClO有强氧化性.
点评:本题考查生电解池的工作原理以及电极反应式的书写和电极上的现象知识,属于基本知识的考查,难度不大.

练习册系列答案
相关题目
实验室用乙酸、乙醇、浓H2SO4制取乙酸乙酯,加热一段时间后,在饱和Na2CO3溶液的上面得到无色油状液体,当振荡混合时,有气泡产生,原因是( )
| A、有部分未反应的乙酸被蒸馏出来 |
| B、有部分未反应的乙醇被蒸馏出来 |
| C、产品中有被蒸馏出的H2SO4 |
| D、有部分乙醇跟浓H2SO4作用生成乙烯 |
某溶液中含有两种溶质NaCl和H2SO4,物质的量之比为3:1.用石墨作电极电解溶液,根据电极产物,可明显分为三个阶段.下列叙述不正确的是( )
| A、阴极只析出H2 |
| B、阳极先析出Cl2,后析出O2 |
| C、电解最后阶段为电解水 |
| D、溶液pH不断增大,最后为7 |
下列有关实验的叙述,正确的是( )
| A、将固体加入容量瓶中溶解并稀释至刻度,配置成一定物质的量浓度的溶液 |
| B、某溶液与BaCl2溶液反应生成白色沉淀,说明原溶液中有SO42- |
| C、用NaOH溶液洗涤并灼烧铂丝后,再进行焰色反应 |
| D、可以用湿润的红色石蕊试纸检验是否有氨气生成 |
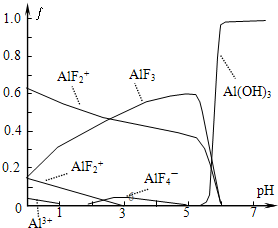 氟和氟盐是化工原料.由于氟气性质活泼,很晚才制取出来.
氟和氟盐是化工原料.由于氟气性质活泼,很晚才制取出来.