题目内容
在恒容的密闭容器中充入2molA和1molB的气体后发生反应2A(g)+B(g)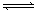 xC(g),达到平衡后,C的体积分数为m%。若维持容器容积和温度不变,按0.6molA、0.3molB和1.4molC为起始物质的量,达到平衡后,C的体积分数仍为m%。则x的值可能为
xC(g),达到平衡后,C的体积分数为m%。若维持容器容积和温度不变,按0.6molA、0.3molB和1.4molC为起始物质的量,达到平衡后,C的体积分数仍为m%。则x的值可能为
A、1 B、2 C、3 D、4
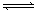 xC(g),达到平衡后,C的体积分数为m%。若维持容器容积和温度不变,按0.6molA、0.3molB和1.4molC为起始物质的量,达到平衡后,C的体积分数仍为m%。则x的值可能为
xC(g),达到平衡后,C的体积分数为m%。若维持容器容积和温度不变,按0.6molA、0.3molB和1.4molC为起始物质的量,达到平衡后,C的体积分数仍为m%。则x的值可能为A、1 B、2 C、3 D、4
BC
略

练习册系列答案
 优质课堂快乐成长系列答案
优质课堂快乐成长系列答案
相关题目
 ,恒容时,温度升高.H2浓度减小。分析下列问题:
,恒容时,温度升高.H2浓度减小。分析下列问题: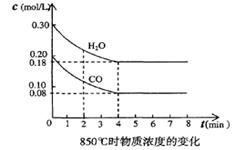
 CO+H2O (g),t时刻容器内各物质的浓度分别为:一氧化碳0.09 mol/L、水蒸气0.09 mol/L、二氧化碳0.08 mol/L、氢气 0.08 mol/L,此时v(正) v(逆)(“大于”“ 小于”“等于”)
CO+H2O (g),t时刻容器内各物质的浓度分别为:一氧化碳0.09 mol/L、水蒸气0.09 mol/L、二氧化碳0.08 mol/L、氢气 0.08 mol/L,此时v(正) v(逆)(“大于”“ 小于”“等于”) 2HI(g)的平衡常数是50,在该温度下只充入H2与I2(g)发生反应,反应开始时,碘蒸气的浓度是1mol·L-1,当达到平衡时c(HI)=0.9mol·L-1,求H2的转化率?(保留三位有效数字)
2HI(g)的平衡常数是50,在该温度下只充入H2与I2(g)发生反应,反应开始时,碘蒸气的浓度是1mol·L-1,当达到平衡时c(HI)=0.9mol·L-1,求H2的转化率?(保留三位有效数字)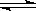 2C3(g);△H=-Q1 kJ/mol(Q1>0),在一个有催化剂的固定
2C3(g);△H=-Q1 kJ/mol(Q1>0),在一个有催化剂的固定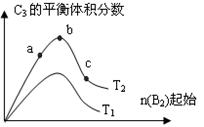
 00℃时充分反应,达平衡后C3的浓度为
00℃时充分反应,达平衡后C3的浓度为 衡后,吸收热量Q3
衡后,吸收热量Q3 kJ,C3浓度 (填>、=、<)w mol/L,Q1、Q2、Q3之间满足何种关系 (用代数式表示)。
kJ,C3浓度 (填>、=、<)w mol/L,Q1、Q2、Q3之间满足何种关系 (用代数式表示)。 器(反应前体积相同),起始时加入2 molA2和l molB2,500℃时充分反应达平衡后,放出热量Q4 kJ,则Q2 Q4 ( 填 > 、 = 、 < ),理由是 。
器(反应前体积相同),起始时加入2 molA2和l molB2,500℃时充分反应达平衡后,放出热量Q4 kJ,则Q2 Q4 ( 填 > 、 = 、 < ),理由是 。 PCl3(g)+Cl2(g) △H>0 K=1 ①
PCl3(g)+Cl2(g) △H>0 K=1 ① 2C(g)+D(g) 已达平衡状态的是 ( )
2C(g)+D(g) 已达平衡状态的是 ( )  2SO3(g)并达到平衡,在此过程中,甲维持容器的体积不变,乙维持容器的压强不变,若甲中SO2的转化率为a%,则对乙中SO2的转化率的合理描述为下列的 ( )
2SO3(g)并达到平衡,在此过程中,甲维持容器的体积不变,乙维持容器的压强不变,若甲中SO2的转化率为a%,则对乙中SO2的转化率的合理描述为下列的 ( )
 2HI(g)。下列叙述能够说明反应已达平衡状态的是
2HI(g)。下列叙述能够说明反应已达平衡状态的是