题目内容
1.下列关于物质性质变化的比较,不正确的是( )| A. | 原子半径大小:Na>S>O | B. | 还原性强弱:F->Cl->Br->I- | ||
| C. | 碱性强弱:KOH>NaOH>LiOH | D. | 气态氢化物稳定性:HBr>HCl>HF |
分析 A.电子层越多,原子半径越大;同周期从左向右原子半径减小;
B.非金属性越强,对应阴离子的还原性越弱;
C.金属性越强,对应最高价氧化物的水化物的碱性越强;
D.非金属性越强,对应气态氢化物越稳定.
解答 解:A.电子层越多,原子半径越大;同周期从左向右原子半径减小,则原子半径大小:Na>S>O,故A正确;
B.非金属性越强,对应阴离子的还原性越弱,则还原性强弱:F-<Cl-<Br-<I-,故B错误;
C.金属性越强,对应最高价氧化物的水化物的碱性越强,则碱性强弱:KOH>NaOH>LiOH,故C正确;
D.非金属性越强,对应气态氢化物越稳定,则气态氢化物稳定性:HBr<HCl<HF,故D错误;
故选BD.
点评 本题考查元素周期律及元素周期表,为高频考点,把握元素的位置、元素的性质及元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
11.下列不属于氧化还原反应的是( )
| A. | S+O2 $\frac{\underline{\;点燃\;}}{\;}$SO2 | B. | Fe(OH)3+3HCl═FeCl3+3H2O | ||
| C. | 2Mg+CO2$\frac{\underline{\;点燃\;}}{\;}$2MgO+C | D. | 4HNO3(浓)$\frac{\underline{\;光照\;}}{\;}$4NO2↑+O2↑+2H2O |
9.NA为阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 1 L 0.2 mol•L-1硫酸铁溶液中含有的SO42-数为0.6NA | |
| B. | 60 g SiO2晶体中含有2NA个Si-O键 | |
| C. | 1L浓度为1mol•L-1的Na2CO3溶液中含有NA个CO32- | |
| D. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA |
16.工业上以碳酸锰矿为主要原料生产MnO2的工艺流程如下:

有关氢氧化物开始沉淀和沉淀完全的pH如下表:
请问答下列问题:
(1)酸浸前将碳酸锰矿粉碎的作用是增大接触面积,加快反应速率(使反应更充分).
(2)酸浸后的溶液中含有Mn2+、SO42-,另含有少量Fe2+、Fe3+、Al3+、Cu2+、Pb2+等,其除杂过程如下:
①加入MnO2将Fe2+氧化,其离子反应方程式为2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
②加入CaO将溶液的pH调到5.2~6.0,其主要目的除去Fe3+,A13+.
③加入BaS,除去Cu2+、Pb2+.

有关氢氧化物开始沉淀和沉淀完全的pH如下表:
| 氢氧化物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 | Pb(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 3.3 | 1.5 | 6.5 | 4.2 | 8.0 | 8.3 |
| 沉淀完全的pH | 5.2 | 3.7 | 9.7 | 6.7 | 8.8 | 9.8 |
(1)酸浸前将碳酸锰矿粉碎的作用是增大接触面积,加快反应速率(使反应更充分).
(2)酸浸后的溶液中含有Mn2+、SO42-,另含有少量Fe2+、Fe3+、Al3+、Cu2+、Pb2+等,其除杂过程如下:
①加入MnO2将Fe2+氧化,其离子反应方程式为2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
②加入CaO将溶液的pH调到5.2~6.0,其主要目的除去Fe3+,A13+.
③加入BaS,除去Cu2+、Pb2+.
13.下列说法错误的是( )
| A. | 煤、石油、天然气是当今世界最重要的三种化石燃料 | |
| B. | 化学反应必然伴随发生能量变化 | |
| C. | 利用生物质能就是间接利用太阳能 | |
| D. | 凡经加热而发生的化学反应都是吸热反应 |
10.实验室有两瓶失去标签的溶液,其中一瓶是食盐水,另一瓶是蔗糖水.以下鉴别方法不正确的是( )
| A. | 在两种溶液中分别加入少量稀硫酸,加热,再加入碱中和硫酸,再加入银氨溶液,水浴加热 | |
| B. | 测量溶液的导电性 | |
| C. | 向两种溶液中分别滴加硝酸银溶液 | |
| D. | 尝味道 |
11.下列说法正确的是( )
| A. | NH3可以用来做喷泉实验是因为其有特殊气味 | |
| B. | 工业上用氨和二氧化碳合成尿素属于氮的固定 | |
| C. | 液氨作制冷剂原因是其气化时大量吸收周围的热量 | |
| D. | NH3能使无色酚酞溶液变红 |
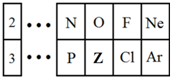 如图是元素周期表的一部分,请回答下列问题.
如图是元素周期表的一部分,请回答下列问题.