题目内容
25℃时,已知弱酸的电离常数:Ki(CH3COOH) = 1.8 ×10-5;Ki1(H2CO3) = 4.4 ×10-7;Ki2(H2CO3) = 4.7 × 10-11;Ki(HClO) = 4.0 ×10-8。则下列说法正确的是
A.物质的量浓度相等的溶液pH关系:pH(NaClO)>pH(Na2CO3)>pH(CH3COONa)
B.向NaClO溶液中通少量CO2:CO2 + NaClO + H2O → NaHCO3 + HClO
C.a mol/L HClO与b mol/L NaOH溶液等体积混合后所得溶液中c(Na+)>c(ClO-),则a一定小于b
D.向氯水中加入NaHCO3固体,可以增大氯水中次氯酸的浓度
BD
【解析】
试题分析:A、电离常数越大酸性越强,则根据电离常数可知酸性强弱顺序是CH3COOH>H2CO3>HCO3->HclO。酸越弱,相应的钠盐越容易水解,溶液碱性越强,则物质的量浓度相等的溶液pH关系:pH(Na2CO3)>pH(NaClO)>pH(CH3COONa),A错误;B、向NaClO溶液中通少量CO2生成碳酸氢钠和次氯酸,即CO2 + NaClO + H2O → NaHCO3 + HclO,B正确;C、a mol/L HClO与b mol/L NaOH溶液等体积混合后所得溶液中c(Na+)>c(ClO-),则根据电荷守恒可知溶液显碱性,二者如果恰好反应生成的次氯酸钠水解溶液也显碱性,因此a不一定小于b,C错误;D、向氯水中加入NaHCO3固体,碳酸氢钠与盐酸反应,但与次氯酸不反应,促进氯气的溶解,因此可以增大氯水中次氯酸的浓度,D正确,答案选BD。
考点:考查电离常数的应用

 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案(本题共12分)葡萄糖酸钙是一种可促进骨骼生长的营养物质。葡萄糖酸钙可通过以下反应制得:C6H12O6(葡萄糖)+Br2+H2O→C6H12O7(葡萄糖酸)+2HBr
2C6H12O7(葡萄糖酸)+CaCO3→ (C6H11O7)2 Ca (葡萄糖酸钙)+H2O+CO2
相关物质的溶解性见下表:
物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
水中的溶解性 | 可溶于冷水 易溶于热水 | 可溶 | 易溶 | 易溶 |
乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |
实验流程如下:
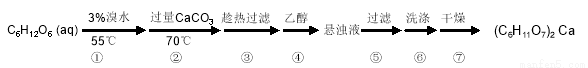
请回答下列问题:
32.第②步中所加CaCO3还发生了其他反应,写出其中一个主要反应的方程式________;充分反应后CaCO3固体需有剩余,目的是______________________;
33.第③步需趁热过滤,原因是______________________;
34.第④步加入乙醇的作用是______________________;
35.第⑥步中,下列洗涤剂最合适的是________。
A.冷水 B.热水 C.乙醇 D.乙醇-水混合溶液
锌是人体健康所必需的元素,葡萄糖酸锌是一种常用的补锌剂,对婴儿及青少年的智力和身体发育有重要作用。工业上以葡萄糖酸钙为原料通过如下两步制备葡萄糖酸锌:

步骤1:充分反应后,过滤除去CaSO4沉淀。步骤2:将葡萄糖酸溶液与ZnO混合。
36.步骤2中,待其充分反应后,须继续加入葡萄糖酸溶液至pH为5.8,目的是 。
37.下列物质可替代ZnO的是 (填字母)。
a.NH3·H2O
b.Zn(OH)2
c.NaOH
d.ZnSO4
e.ZnCO3



