题目内容
14.元素周期表前10种元素中,可构成含4个原子核及10个电子的粒子(不含同位素原子)共有( )| A. | 2种 | B. | 4种 | C. | 5种 | D. | 8种 |
分析 元素周期表前10种元素中,四核10电子的微粒有:NH3、H3O+来解答.
解答 解:元素周期表前10种元素中,可构成含4个原子核及10个电子的粒子(不含同位素原子)共有2种:NH3、H3O+,故选A.
点评 本题考查核外电子排布,比较基础,注意核外电子数目的计算是解题的关键.

练习册系列答案
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案
相关题目
5.关于葡萄糖的说法中,下列错误的是( )
| A. | 葡萄糖的分子式是C6H12O6 | |
| B. | 葡萄糖是一种多羟基醛,因而具有醛和多元醇的性质 | |
| C. | 葡萄糖能水解 | |
| D. | 葡萄糖可被还原为己六醇 |
2.下列各种材料属于新型无机非金属材料的是( )
| A. | 陶瓷 | B. | 水泥 | C. | 玻璃 | D. | 光导纤维 |
9.下列说法正确的是( )
| A. | 二氧化硅既不溶于水也不溶于任何酸 | |
| B. | 二氧化碳通入饱和氯化钙溶液中能生成白色沉淀 | |
| C. | 二氧化碳通入硅酸钠溶液中可以得到硅酸 | |
| D. | 二氧化硅是制造玻璃的主要原料,它不能与氢氧化钠溶液反应 |
6.下列叙述正确的是( )
| A. | 摩尔是表示物质的量的多少的基本物理量 | |
| B. | 0.012kg12C中含有约6.02×1023个碳原子 | |
| C. | 氢氧化钠的摩尔质量是40g | |
| D. | 2mol水的摩尔质量是1mol水的摩尔质量的2倍 |
7.下面的排序不正确的是( )
| A. | 含氧酸酸性强弱:HClO4>HClO3>HClO2>HClO | |
| B. | 硬度由大到小:金刚石>碳化硅>晶体硅 | |
| C. | 熔点由高到低:Na>Mg>Al | |
| D. | 晶格能由大到小:NaF>NaCl>NaBr>NaI |
8.NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 1molCl2与足量的NaOH溶液完全反应,转移的电子数是2NA | |
| B. | 50mL12mol/L盐酸与足量MnO2共热,转移的电子数为0.3NA | |
| C. | 密闭容器中2mo1NO与1molO2充分反应,容器中的分子数为2NA | |
| D. | 过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA |
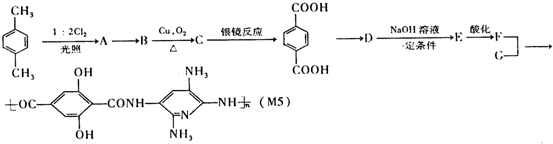
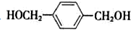 ;合成M5的单体的结构简式:F
;合成M5的单体的结构简式:F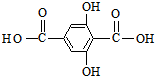 ,G
,G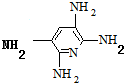 ;
;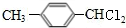 ;
;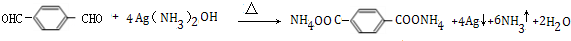 .
.