题目内容
20.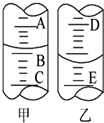 (1)①如图甲表示10mL量筒中液面的位置,A与B、B与C刻度间相差1mL,如果刻度A为4,量筒中液体的体积是3.2mL.
(1)①如图甲表示10mL量筒中液面的位置,A与B、B与C刻度间相差1mL,如果刻度A为4,量筒中液体的体积是3.2mL.②如图乙表示50 mL滴定管中液面的位置,如果液面处的读数是a,则滴定管中液体的体积(填代号)D.
A.是a mL B.一定大于a mL
C.是(50-a) mL D.一定大于(50-a) mL
(2)加热蒸干Al2(SO4)3溶液,最后得到的主要固体产物是Al2(SO4)3(填化学式,下同);把FeCl2溶液蒸干,并进一步灼烧,最后得到的主要固体产物是Fe2O3.
分析 (1)①量筒小刻度在下,A与B与C刻度间相差1mL,刻度A为4,则刻度B为3,AB间每一小格为0.2mL,则量筒中液体的体积为3.2mL;
②液面处的读数是aml,则有读数部分的液体体积为(50-a)mL,滴定管下端有一定没有刻度,滴定管内液体的体积大于(50-a)mL;
(2)硫酸铝在水中水解生成氢氧化铝和硫酸,硫酸为难挥发性酸;根据三氯化铁在溶液中存在水解平衡,从平衡移动的角度分析并解答该题.
解答 解:(1)①量筒小刻度在下,A与B与C刻度间相差1mL,刻度A为4,则刻度B为3,AB间每一小格为0.2mL,则量筒中液体的体积为3.2mL,故答案为:3.2;
②液面处的读数是aml,则有读数部分的液体体积为(50-a)mL,滴定管下端有一定没有刻度,滴定管内液体的体积大于(50-a)mL,
故答案为:D;
(2)硫酸铝在水中水解生成氢氧化铝和硫酸,硫酸为难挥发性酸,所以最终得到的产物是硫酸铝,在FeCl3溶液中,Fe3+发生水解生成Fe(OH)3:FeCl3+3H2O?Fe(OH)3+3HCl,由于加热蒸发,使HCl挥发,破坏平衡,使平衡不断向右移动,结果生成Fe(OH)3,又由于灼热发生2Fe(OH)3$\frac{\underline{\;\;△\;\;}}{\;}$Fe2O3+3H2O,使Fe(OH)3分解生成Fe2O3,
故答案为:Al2(SO4)3;Fe2O3.
点评 本题考查了常用仪器的使用和盐的水解的应用知识,可以根据所学知识进行回答,难度中等,平时注意知识的积累.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
10.甲、乙、丙、丁四种物质中,甲、乙、丙均含有相同的某种元素,它们之间具有如下转化关系:甲$\stackrel{丁}{→}$乙$?_{甲}^{丁}$丙,下列有关物质的推断不正确的是( )
| A. | 若甲为Fe,则丁可能是Cl2 | B. | 若甲为焦炭,则丁可能是O2 | ||
| C. | 若甲为SO2,则丁可能是氨水 | D. | 若甲为NaOH 溶液,则丁可能是CO2 |
11.在一密闭容器中存在如下反应:2SO2(g)+O2(g)?2SO3(g)△H<0.某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,下列分析错误的是( )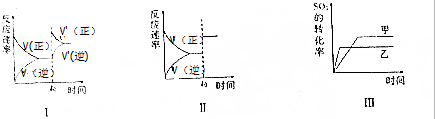

| A. | 图Ⅰ研究的是t0时刻增大O2的浓度对反应速率的影响 | |
| B. | 图Ⅱ研究的是t0时刻加入催化剂后对反应速率的影响 | |
| C. | 图Ⅲ研究的是压强对化学平衡的影响,且乙的压强比甲高 | |
| D. | 图Ⅲ研究的是温度对化学平衡的影响,且乙的温度比甲高 |
8.如图表示水溶液中c(H+)和c(OH-)的关系,下列判断正确的是( )
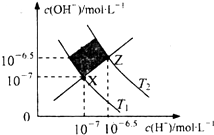

| A. | XZ线上任意点均表示溶液的pH=7 | |
| B. | 图中T1>T2 | |
| C. | M区域对应溶液中大量存在:Fe3+、Na+、C1-、SO42- | |
| D. | Z点对应的可能是CH3COOH和CH3COONa的混合液,且c(CH3COO-)=c(Na+) |
15.下列各组物质全部是弱电解质的是( )
| A. | H2SiO3. H2S CO2 | B. | H2O NH3•H2O HClO HF | ||
| C. | H2SO3. Ba(OH)2 BaSO4 | D. | H2SO3. Ba(OH)2 BaSO4 |
5.下列叙述I和II均正确并有因果关系的是( )
| 选项 | 叙述I | 叙述II |
| A | 用酸度计测定SO2和CO2饱和溶液的pH,前者pH小 | 结论:说明H2SO3酸性强于H2CO3 |
| B | SiO2是酸性氧化物 | SiO2不与任何酸溶液反应 |
| C | 配制SnCl2溶液时,先将SnCl2溶于适量的稀盐酸中,再用蒸馏水稀释,保存时再在试剂瓶中加入少量的锡粒 | 抑制Sn2+水解,并防止Sn2+被氧化为Sn4+ |
| D | 浓硝酸具有强氧化性 | 应保存在棕色玻璃试剂瓶中 |
| A. | A | B. | B | C. | C | D. | D |
12.利用辉铜矿冶炼铜时发生的主要反应为Cu2S+O2$\frac{\underline{\;高温\;}}{\;}$2Cu+SO2,该反应属于( )
| A. | 分解反应 | B. | 复分解反应 | C. | 置换反应 | D. | 化合反应 |
9.设NA代表阿伏加德罗常数的值,下列说法正确的是( )
| A. | 常温常压下,11.2L氧气所含的氧原子数为NA | |
| B. | 2.4g镁变成Mg2+时失去的电子数为0.2NA | |
| C. | 1mol•L-1的CaCl2溶液中含有的Cl-数为2NA | |
| D. | 标准状况下,2g氢气所含氢原子数为NA |
10.化学与生产、生活、社会密切相关.下列说法不正确的是 ( )
| A. | 面粉加工厂、铝制品抛光车间须严格控制粉尘浓度以防爆炸 | |
| B. | 甲醇燃料电池的能量转换效率远高于甲醇燃烧的能量转换效率 | |
| C. | 为了保证食品的安全与色香味统一,应全面禁止使用食品添加剂 | |
| D. | 石墨烯是一种由单层碳原子构成的新纳米材料,具有导电性 |