题目内容
能正确表示下列反应的离子反应方程式为( )
| A、NH4HCO3溶于过量的浓KOH溶液中:NH4++HCO3-+2OH-═CO32-+NH3↑+2 H2O |
| B、向明矾溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -═2 Al(OH)3↓+3BaSO4↓ |
| C、向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2═2 Fe3++2Br2+6 Cl- |
| D、醋酸除去水垢:2H++CaCO3═Ca2++CO2↑+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.反应生成碳酸钾、氨气、水;
B.恰好使SO42-沉淀完全,以1:2反应,反应生成硫酸钡、偏铝酸钾;
C.足量氯气,亚铁离子、溴离子均被氧化;
D.醋酸在离子反应中保留化学式.
B.恰好使SO42-沉淀完全,以1:2反应,反应生成硫酸钡、偏铝酸钾;
C.足量氯气,亚铁离子、溴离子均被氧化;
D.醋酸在离子反应中保留化学式.
解答:
解:A.NH4HCO3溶于过量的浓KOH溶液中的离子反应为NH4++HCO3-+2OH-═CO32-+NH3↑+2H2O,故A选;
B.明矾溶液中Al3+和SO42-个数比为1:2,SO42-完全沉淀时,Al3+应转化为AlO2-,离子反应为Al3++2SO42-+2Ba2++4OH -═AlO2+2H2O+2BaSO4↓故B不选;
C.向FeBr2溶液中通入足量氯气的离子反应为2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-,故C选;
D.醋酸是弱酸,则醋酸除去水垢的离子反应为2HAc+CaCO3═Ca2++CO2↑+H2O+2Ac-,故D不选;
故选AC.
B.明矾溶液中Al3+和SO42-个数比为1:2,SO42-完全沉淀时,Al3+应转化为AlO2-,离子反应为Al3++2SO42-+2Ba2++4OH -═AlO2+2H2O+2BaSO4↓故B不选;
C.向FeBr2溶液中通入足量氯气的离子反应为2Fe2++4Br-+3Cl2═2Fe3++2Br2+6Cl-,故C选;
D.醋酸是弱酸,则醋酸除去水垢的离子反应为2HAc+CaCO3═Ca2++CO2↑+H2O+2Ac-,故D不选;
故选AC.
点评:本题考查离子方程式的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重氧化还原反应及与量有关的离子反应的考查,题目难度不大.

练习册系列答案
相关题目
金刚石和石墨是由碳元素组成的两种结构不同的单质(同素异形体).在100kPa时,1 mol石墨转化为金刚石,要吸收1.895kJ的热能.据此,试判断在100kPa压强下,下列结论正确的是( )
| A、石墨比金刚石稳定 |
| B、金刚石比石墨稳定 |
| C、1 mol石墨比1 mol 金刚石的总能量高 |
| D、1 mol金刚石比1 mol 石墨的总能量高 |
在卤族元素中非金属性最强的是( )
| A、F | B、Cl | C、Br | D、I |
NA为阿伏加德罗常数,下列说法正确的是( )
| A、1Llmol/L的Na2CO3溶液中含有的CO32-数目为NA |
| B、1mol羟基(-OH)所含的电子数约为l0NA |
| C、1mol丙烯分子有2molσ键,1molπ键 |
| D、现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
下列家庭化学小实验不能达到预期目的是( )
| A、用灼烧并闻气味的方法区别纯棉织物和纯羊毛织物 |
| B、用食醋、石灰水验证蛋壳中含有碳酸盐 |
| C、用米汤检验食用加碘盐(含KIO3)中含有碘 |
| D、用鸡蛋白、食盐、水完成蛋白质的溶解、盐析实验 |
两种气态烃的混合气共1mol,在空气中燃烧得到1.5molCO2和2molH2O.关于该混合气的说法合理的是( )
| A、一定含甲烷,不含乙烷 |
| B、一定含乙烷,不含甲烷 |
| C、可能是甲烷和乙烯的混合物 |
| D、一定含甲烷,但不含乙烯 |
有一定体积CH4、C2H6、C3H8组成的混合气体,是同温同压下H2密度的15倍.则混合气体中CH4、C2H6、C3H8的体积比不可能是( )
| A、2:1:2 |
| B、2:3:1 |
| C、1:4:1 |
| D、5:3:5 |
将m g二氧化锰与一定体积的浓盐酸反应,得到n L氯气(标准状况).可确定该反应中被氧化的浓盐酸中HCl的物质的量一定正确的是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
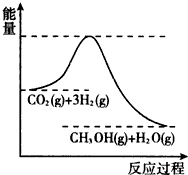 由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),该反应的能量变化如图所示:
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视.目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),该反应的能量变化如图所示: