题目内容
9.下列操作正确的是( )| A. | pH试纸直接蘸取NaOH溶液测定其pH | |
| B. | 存放化学品的仓库失火后,尽快用水灭火 | |
| C. | 蒸馏时,加热一段时间后,再投入沸石 | |
| D. | 切割剩下的白磷放回原试剂瓶水封保存 |
分析 A.应用玻璃棒蘸取溶液;
B.如化学品与水反应,则不能用水灭火;
C.应先加入沸石;
D.白磷易燃,应避免失火.
解答 解:A.pH试纸直接蘸取NaOH溶液,易导致污染,应用玻璃棒蘸取溶液滴在试纸上,故A错误;
B.如化学品与水反应,则不能用水灭火,故B错误;
C.应先加入沸石,避免暴沸,故C错误;
D.白磷易燃,应避免失火,不能随意丢弃,应放回原试剂瓶水封保存,故D正确.
故选D.
点评 本题考查较为综合,涉及pH试纸的使用、实验安全问题、操作等问题,为高考常见题型,侧重考查学生的分析能力和实验能力,注意把握物质的性质以及实验的严密性和可行性的评价,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.下列说法正确的是( )
| A. | 常温常压下,1mol任何气体的体积都约是22.4L | |
| B. | 标准状况下,气体的摩尔体积约是22.4L | |
| C. | 0℃,101kpa时,2gH2的体积约是22.4L | |
| D. | 标准状况下,1mol水的体积约是22.4L |
10.下列各澄清溶液中离了能大量共存,且加入(或滴入)X试剂后发反应的离子方程式书写正确的是( )
| 选项 | 离子组 | X试剂 | 离子方程式 |
| A | Na+、K+、ClOˉ、SO42ˉ | 少量SO2 | 2ClOˉ+SO2+H2O═2HClO+SO32ˉ |
| B | NH4+、Fe3+、Brˉ、SO42ˉ | 过量H2S | 2Fe3++H2S=2Fe2++S↓+2H+ |
| C | NH4+、Na+、Fe3+、AlO2- | 过量铜粉 | Cu+2Fe3+═2Fe2++Cu2+ |
| D | Na+、K+、HCO3-、AlO2- | 少量HCl | H++AlO2-+H20═Al(OH)3↓ |
| A. | A | B. | B | C. | C | D. | D |
4.下列说法不正确的是( )
| A. | 化学反应速率的大小主要由浓度、温度、压强等外界因素决定 | |
| B. | 化石燃料是不可再生能源,生物质能是可再生能源 | |
| C. | 许多水果与花卉的芳香气味是因含有酯的原因 | |
| D. | 人工合成尿素,彻底动摇了“生命力论”,使有机化学迅猛发展 |
18.下列叙述正确的是( )
| A. | 1 mol H2O的质量为18 g•mol-1 | |
| B. | CH4的摩尔质量为16 g | |
| C. | 3.01×1023个SO2分子的质量为32 g | |
| D. | 1 mol NaCl溶于1 L水中,形成1 mol•L-1NaCl溶液 |
19.如图是工业“从海水中提取镁”的简易流程示意图.下列说法中不正确的是( )
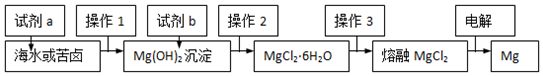

| A. | 流程中试剂a为NaOH溶液,试剂b为盐酸 | |
| B. | 操作2的具体方法是加热浓缩,冷却结晶 | |
| C. | 操作3是将晶体置于HCl气体氛围中脱水 | |
| D. | 电解MgCl2时,阳极生成Cl2,阴极生成Mg |