题目内容
孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物。实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下:
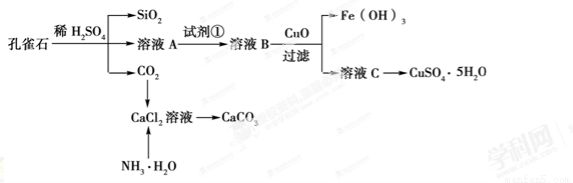
请回答下列问题:
(1)溶液A中的金属离子有Cu2+、Fe2+、Fe3+。从下列所给试剂中选择:实验步骤中试剂①为________(填代号),检验溶液A中Fe3+的最佳试剂为________(填代号)。
a.KMnO4 b.(NH4)2S
c.H2O2 d.KSCN
(2)由溶液C获得CuSO4·5H2O,需要经过加热蒸发、________、过滤等操作。除烧杯、漏斗外,过滤操作还用到另一玻璃仪器,该仪器在此操作中的主要作用是________。
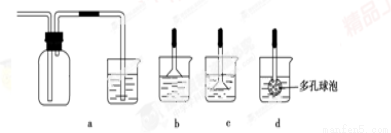
(3)制备CaCO3时,应向CaCl2溶液中先通入(或先加入)________(填化学式)。若实验过程中有氨气逸出,应选用下列________装置回收(填代号)。
(4)欲测定溶液A中Fe2+浓度,需要用容量瓶配制某标准溶液,定容时视线应____________,直到__________。用KMnO4标准溶液滴定时应选用__________滴定管(填“酸式”或“碱式”)。
(每空2分共18分)
(1)c;d (2)冷却结晶;引流 (3)NH3(或NH3?H2O);b
(4)平视凹液面(或与刻度线相平),溶液凹液面最低处与刻度线相切;酸式
【解析】
试题分析:(1)本实验要除去Fe2+、Fe3+等离子,先加入合适的氧化剂时不能引入新的杂质,可加入H2O2,发生的反应为:2H2O2+2Fe2++2H+═2Fe3++4H2O,因Fe3+遇KSCN溶液变为血红色,则可用KSCN检验Fe3+,故答案为:c;d。
(2)从溶液中要析出晶体,采用冷却结晶法,然后进行过滤等操作,过滤用到的仪器有烧杯、玻璃棒、漏斗、滤纸等仪器,其中玻璃棒在过滤时起到引流的作用,。
(3)CaCl2溶液不能与CO2反应,加入碱能反应,但又不能引入杂质,应通入NH3,实验室收集氨气时要注意防止倒吸,因为氨气极易溶于水,吸收时导管不能插入到液面以下,可用倒置的漏斗,故答案为:NH3?H2O;b。
(4)读数时不能人为带来误差,视线要与刻度线相平,溶液凹液面最低处与刻度线相切,又高锰酸钾具有强氧化性,则只能用酸式滴定管盛装高锰酸钾溶液,故答案为:与刻度线相平,溶液凹液面最低处与刻度线相切;酸式。
考点:本题考查化学流程的分析、实验基本操作、物质的制取和提纯、离子的检验。

(15分)新型材料纳米级铁粉与普通铁粉具有不同的性质。已知:在不同温度下,纳米级铁粉与水蒸气反应的固体产物不同,温度低于570℃时,生成FeO;高于570℃时,生成Fe3O4。
(1)写出温度高于570℃时反应的化学方程式
。
(2)中学教材中用下图所示实验装置,完成铁粉与水蒸气反应的演示实验。实验中使用肥皂液的作用是 。
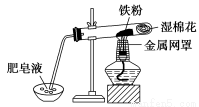
(3)如果提供给你3支试管、水槽、蒸发皿、胶塞、导管、酒精灯及其必要的仪器和物品,请在答题卷的方框中画出你设计的实验装置示意图(包括反应时容器中的物质)。
说明:①本题装置示意图中的仪器可以用下面的方式表示。
水槽: 试管:
试管: 蒸发皿:
蒸发皿: 玻璃导管:
玻璃导管: 或
或 (但应标示出在液面上或液面下)
(但应标示出在液面上或液面下)
②铁架台、石棉网、酒精灯、玻璃导管之间的联接胶管等,在示意图中不必画出。如需加热,在需加热的仪器下方,标以“△”表示。
(4)甲同学对实验后的黑色固体产物X含有哪些物质进行了如下实验:
实验步骤 | 实验操作 | 实验现象 |
Ⅰ | 取少量黑色固体产物X(假定成分分布均匀)放入试管中,加入盐酸,微热。 | 黑色粉末逐渐溶解,有少量气泡产生。 |
Ⅱ | 取实验Ⅰ反应后的溶液少许,滴加几滴KSCN溶液,振荡。 | 溶液没有出现血红色。 |
Ⅲ | 取实验Ⅰ反应后的溶液少许,滴加几滴酸性KMnO4溶液,振荡。 | 高锰酸钾溶液褪色。 |
根据以上实验事实,能确定固体X中存在的物质是 ,但不能确定X的成分,原因是 。
(5)乙同学为了探究实验后的固体产物是否存在Fe3O4设计下列实验方案:
①取固体样品m1 g,溶于足量的稀盐酸;
②向①反应后的溶液中加入足量H2O2的和氨水,充分反应后,过滤、洗涤、干燥;
③将②中所得固体进行灼烧,得到红棕色固体m2 g。
溶液X中发生氧化还原反应的离子方程式为 ;m1与m2的比值在 范围内时,才能确定固体样品中一定存在Fe3O4。
(15分)高铁酸钾(K2FeO4)是一种高效多功能水处理剂,具有极强的氧化性。
(1)已知:4FeO42-+10H2O 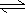 4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有 。
4Fe(OH) 3+8OH-+3O2↑。K2FeO4在处理水的过程中所起的作用有 。
同浓度的高铁酸钾在pH为4.74、7.00、11.50的水溶液中最稳定的是pH= 的溶液。
(2)高铁酸钾有以下几种常见制备方法:
干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
电解法 | 制备中间产物Na2FeO4,再与KOH溶液反应 |
①干法制备K2FeO4的反应中,氧化剂与还原剂的物质的量之比为____ 。
②湿法制备中,若Fe(NO3)3加入过量,在碱性介质中K2FeO4与Fe3+发生氧化还原反应生成K3FeO4,此反应的离子方程式:____ ________________。
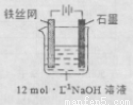
③制备中间产物Na2FeO4,可采用的装置如图所示,则阳极的电极反应
式为 。
(3)比亚迪双模电动汽车使用高铁电池供电,其总反应为:
3Zn+2K2FeO4+8H2O 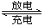 3Zn(OH)2+2Fe(OH)3+4KOH
3Zn(OH)2+2Fe(OH)3+4KOH
放电时负极材料为____ ,正极反应为:____ 。
(4) 25℃时,CaFeO4的Ksp=4.54×l0-9,若要使1000 L含有2.0×l0-4 mol·L-l K2FeO4的废水中的c(FeO42-)有沉淀产生,理论上至少加入Ca(OH)2的物质的量为____ mol。
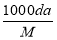
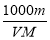 D.a%=
D.a%=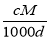 %
%