题目内容
2.铵明矾NH4Al(SO4)2•12H2O是分析化学常用基准试剂,其制备过程如下.下列分析不正确的是( )
| A. | 过程I反应:2NH4HCO3+Na2SO4═2NaHCO3↓+(NH4)2SO4 | |
| B. | 检验溶液B中阴离子的试剂仅需BaCl2溶液 | |
| C. | 若省略过程II则铵明矾产率明显减小 | |
| D. | 向铵明矾溶液中逐滴加入NaOH溶液先后观察到:刺激性气体逸出→白色沉淀生成→白色沉淀消失 |
分析 NaHCO3的溶解度较小,所以在饱和碳酸氢铵溶液中加入过量的硫酸钠溶液会产生NaHCO3沉淀,过滤后得滤液中有(NH4)2SO4和少量的NaHCO3,将(NH4)2SO4溶液用稀硫酸调节pH值为2,使NaHCO3生成硫酸钠,得溶液B为(NH4)2SO4溶液和少量的硫酸钠溶液,在B溶液中加入硫酸铝可得铵明矾,据此答题.
解答 解:NaHCO3的溶解度较小,所以在饱和碳酸氢铵溶液中加入过量的硫酸钠溶液会产生NaHCO3沉淀,过滤后得滤液中有(NH4)2SO4和少量的NaHCO3,将(NH4)2SO4溶液用稀硫酸调节pH值为2,使NaHCO3生成硫酸钠,得溶液B为(NH4)2SO4溶液和少量的硫酸钠溶液,在B溶液中加入硫酸铝可得铵明矾,
A、根据上面的分析可知,过程I反应为2NH4HCO3+Na2SO4═2NaHCO3↓+(NH4)2SO4,故A正确;
B、B为(NH4)2SO4溶液和少量的硫酸钠溶液,阴离子为硫酸根离子,且溶液呈酸性,所以检验溶液B中阴离子的试剂仅需BaCl2溶液,故B正确;
C、若省略过程II,则溶液中不少量的碳酸氢钠,会与硫酸铝发生双水解,使铵明矾产率明显减小,故C正确;
D、向铵明矾溶液中逐滴加入NaOH溶液,先有氢氧化铝沉淀产生,后产生氨气,再后来氢氧化钠与氢氧化铝反应,沉淀消失,所以观察到:白色沉淀生成→刺激性气体逸出→白色沉淀消,故D错误,
故选D.
点评 本题考查工艺流程、离子检验、盐类水解、对条件的控制选择、物质的分离提纯等,理解工艺流程原理是解题的关键,是对学生综合能力的考查,需要学生具备扎实的基础与灵活运用能力,题目难度中等.

练习册系列答案
相关题目
14.铝与稀硫酸的反应中,已知30s末硫酸铝的浓度增加了1.2mol/L,若不考虑反应过程中溶液体积的变化,则30s内生成硫酸铝的平均反应速率是( )
| A. | 0.02 mol/(L•s) | B. | 3.6 mol/(L•s) | C. | 1.2 mol/(L•s) | D. | 0.04mol/(L•s) |
11.已知: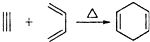 ,如果要合成
,如果要合成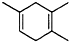 所用的原始原料可以是( )
所用的原始原料可以是( )
①2-甲基-1,3-丁二烯和2-丁炔 ②1,3-戊二烯和2-丁炔
③2,3-二甲基-1,3-戊二烯和乙炔 ④2,3-二甲基-1,3-丁二烯和丙炔.
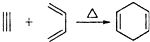 ,如果要合成
,如果要合成 所用的原始原料可以是( )
所用的原始原料可以是( )①2-甲基-1,3-丁二烯和2-丁炔 ②1,3-戊二烯和2-丁炔
③2,3-二甲基-1,3-戊二烯和乙炔 ④2,3-二甲基-1,3-丁二烯和丙炔.
| A. | 只有① | B. | ②③ | C. | ②④ | D. | ①④ |
12.室温下进行的下列实验,不能达到预期目的是( )
| 序号 | 实验内容 | 实验目的 |
| A | 在滴有酚酞的Na2CO3溶液中,滴加入BaC12溶液,溶液红色逐渐褪去 | 证明Na2CO3溶液中存在水解平衡 |
| B | 将Al泊插入浓硝酸中,无现象 | 证明Al和浓硝酸不反应 |
| C | 将两个完全相同且充满NO2的密闭烧瓶,分别浸泡于热水、冰水中 | 探究温度对化学平衡状态的影响 |
| D | 向同体积同浓度的H2O2溶液中,分别加入1mL同浓度的CuSO4、FeCl3溶液 | 比较Cu2+、Fe3+对H2O2分解速率的影响 |
| A. | A | B. | B | C. | C | D. | D |
