题目内容
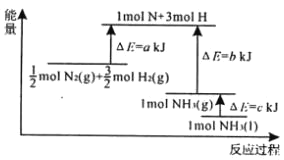
【题目】根据合成氨反应的能量变化示意图,下列有关说法正确的是( )
A.断裂0.5molN2(g)和1.5mol H2(g)中所有的化学键释放a kJ热量
B.NH3(g)═NH3(l)△H=c kJmol﹣1
C.N2(g)+3H2(g)2NH3(g)△H=﹣2(a﹣b)kJmol﹣1
D.2NH3(l)N2(g)+3H2(g)△H=2(b+c﹣a) kJmol﹣1
【答案】D
【解析】
由图可知,断裂化学键吸收akJ热量,形成1mol气态氨气时放热为bkJ,1mol气态氨气转化为液态氨气放出热量为ckJ。
A.断裂0.5mol N2(g)和1.5mol H2(g)中所有的化学键,吸收a kJ热量,故A错误;
B.NH3(g)═NH3(l)△H=﹣c kJmol﹣1,故B错误;
C.由图可知,N2(g)+3H2(g)2NH3(g)△H=2(a﹣b)kJmol﹣1,故C错误;
D.由图可知,N2(g)+3H2(g)2NH3(l)△H=2(a﹣b﹣c)kJmol﹣1,互为逆反应时,焓变的数值相同、符号相反,则2NH3(l)N2(g)+3H2(g)△H=2(b+c﹣a) kJmol﹣1,故D正确;
故选:D。

 阅读快车系列答案
阅读快车系列答案【题目】温度为T时,向2.0L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)![]() PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
PCl3(g)+Cl2(g)经一段时间后达到平衡。反应过程中测定的部分数据见下表:下列说法正确的是
t/s | 0 | 50 | 150 | 250 | 350 |
n(PCl3)/ mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
A.反应在前50 s的平均速率为v(PCl3)=0.0032mol·L-1·s-1
B.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11mol·L-1,则反应的△H<0
C.相同温度下,起始时向容器中充入1.0mol PCl5、0.20mol PCl3和0.20molCl2,达到平衡前v(正)>v(逆)
D.相同温度下,起始时向容器中充入2.0mol PCl3和2.0molCl2,达到平衡时,PCl3的转化率小于80%
【题目】将一定量的CO2气体通入500 mL某氢氧化钠溶液中,充分反应后将溶液在低温下蒸发,得到不含结晶水的白色固体A,取三份质量不相同的A试样分别与50mL相同浓度的盐酸溶液反应,得到标准状况下气体体积与固体A的质量关系如表所示:
组别 | ① | ② | ③ |
A的质量 | 3.80 | 5.70 | 7.60 |
气体体积(mL) | 896 | 1344 | 1120 |
(1)试判断:A的成分___。
(2)盐酸物质的量浓度为___molL﹣1。