题目内容
12.羰基硫(COS)可作为一种熏蒸剂,能防止某些昆虫、线虫的危害.在恒容密闭容器中,将CO和H2S混合加热并达到下列平衡:CO(g)+H2S(g)?COS(g)+H2(g) K=0.1,反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,下列说法正确的是( )| A. | 升高温度,H2S浓度增加,表明该反应是放热反应 | |
| B. | 通入CO后,正反应速率逐渐增大 | |
| C. | 反应前H2S物质的量为7mol | |
| D. | CO的平衡转化率为80% |
分析 A.升高温度,H2S浓度增加,说明平衡逆向移动,升高温度,平衡向吸热反应方向移动;
B.通入CO后,正反应速率瞬间增大,又逐渐减小;
C.反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,设反应前H2S物质的量为n,则:
CO(g)+H2S(g)?COS(g)+H2(g)
起始(mol):10 n 0 0
变化(mol):2 2 2 2
平衡(mol):8 n-2 2 2
反应恰好气体分子数目不变,利用物质的量代替浓度代入平衡常数表达式计算;
D.根据C中的计算数据计算CO的平衡转化率.
解答 解:A.升高温度,H2S浓度增加,说明平衡逆向移动,升高温度,平衡向吸热反应方向移动,则该反应是放热反应,故A正确;
B.通入CO后,正反应速率瞬间增大,又逐渐减小,故B错误;C.反应前CO的物质的量为10mol,平衡后CO物质的量为8mol,设反应前H2S物质的量为n,则:CO(g)+H2S(g)?COS(g)+H2(g)
起始(mol):10 n 0 0
变化(mol):2 2 2 2
平衡(mol):8 n-2 2 2
反应恰好气体分子数目不变,可以利用物质的量代替浓度计算平衡常数,则平衡常数K=$\frac{2×2}{8×(n-2)}$=0.1,解得:n=7,故C正确;
D.根据上述数据,可知CO的平衡转化率为:$\frac{2mol}{10mol}$×100%=20%,故D错误;
故选AC.
点评 本题考查化学平衡的计算,题目难度中等,涉及影响化学反应速率的因素、化学平衡常数应用、化学平衡的有关计算,注意理解掌握三段式均解题法在化学平衡计算中的应用,试题培养了学生的分析能力及化学计算能力.

 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案| A. | 二氧化碳的结构式:O=C=O | |
| B. | 硫酸的电离方程式:H2SO4=H++SO42- | |
| C. | Cl-的结构示意图: | |
| D. | HF的电子式:H+ |
 下表给出五种短周期元素的相关信息.
下表给出五种短周期元素的相关信息.| 元素 | 相关信息 |
| A | 常温、常压下,其单质是最轻的气体,它将成为备受青睐的清洁燃料 |
| B | 工业上通过分离液态空气获得其单质,其某种同素异形体是保护地球地表环境的重要屏障 |
| C | 植物生长三要素之一,它能形成多种氧化物,某些氧化物会造成光化学污染 |
| D | 室温下其单质为淡黄色粉末状固体,加热易熔化.该单质在氧气中燃烧,发出明亮的蓝紫色火焰 |
| E | 常温下其单质为黄绿色气体,其单质水溶液有漂白、杀菌作用 |
(1)D元素核外电子排布
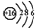 ;
;(2)A、B两元素形成的含有非极性键的化合物的结构式H-O-O-H;A、B两元素形成的具有相同电子数的离子有(填化学式):OH-、H3O+.
(3)C与A形成的某一化合物能和C与B形成的另一无色化合物(这两种化合物分子中原子个数比皆为1:2)一起用作火箭助推剂,两者发生反应生成无毒物质,写出上述化学反应方程式:2N2H4+N2O4═3N2+4H2O.
(4)一定条件下,在水溶液中1mol E-、EO${\;}_{x}^{-}$(x=1,2,3,4)的能量(kJ)相对大小如右图所示.n是ClO4-(填离子符号).离子反应y→x+m的热化学方程式为3ClO-(aq)=2Cl-(aq)+ClO3-(aq)△H=-117kJ•mol-1(用离子符号表示).
(5)Na2DB3水溶液中各离子浓度的大小顺序是Na+>SO32->OH->HSO3->H+(填离子符号)
| A. | 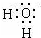 | B. |  | C. | 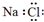 | D. | 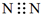 |
| A. | 含氧酸的酸性H3ZO4>H2YO4>HXO4 | |
| B. | HXO4、H2YO4、H3ZO4一定都是强酸 | |
| C. | 元素的负化合价的绝对值按X、Y、Z减小 | |
| D. | 气态氢化物的稳定性按X、Y、Z的顺序减弱 |
 化学反应与能量有着密不可分的关系,回答下列问题.
化学反应与能量有着密不可分的关系,回答下列问题.(1)居民使用的管道煤气主要成分是H2、CO和少量CH4,H2、CO和CH4的燃烧热(注:燃烧热是指在25℃,101kPa时,1mol可燃物质完全燃烧生成稳定的氧化物时所放出的热量,单位为kJ/mol.)数据如表:
| 物质 | H2 | CO | CH4 |
| 燃烧热(kJ•mol-1) | 285.8 | 283.0 | 890.0 |
(2)燃料电池是一种高效、环境友好的发电装置.氢氧燃料电池已用于航天飞机.以氢氧化钾溶液为电解质溶液的这种电池的负极反应式为2H2+4OH--4e-═4H2O,这种电池在放电使用一段时间后,电解质溶液中的c(OHˉ)将减小(填“增大”“减小”或“不变”).
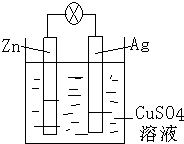
(3)如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液.回答下列问题:
锌为负极,该电极上发生氧化反应(“氧化”或“还原”),电极反应式为Zn-2e-=Zn2+,该原电池的总反应离子方程式为Zn+Cu2+=Cu+Zn2+.