题目内容
人们常用 来表示空气质量.它是根据空气中 、 和 等污染物的浓度计算出来的数值.
考点:常见的生活环境的污染及治理
专题:化学应用
分析:人们常用表示空气的质量,污染指数越大,说明污染越严重,可吸入悬浮颗粒物(浮尘)、二氧化氮、二氧化硫都是对人体有害的污染物.
解答:
解:空气污染指数(Air pollution Index,简称API)就是将常规监测的几种空气污染物浓度简化成为单一的概念性指数值形式,并分级表征空气污染程度和空气质量状况,适合于表示城市的短期空气质量状况和变化趋势.空气污染的污染物有:烟尘、总悬浮颗粒物、可吸入悬浮颗粒物(浮尘)、二氧化氮、二氧化硫、一氧化碳、臭氧、挥发性有机化合物等等.
故答案为:空气污染指数(API);二氧化硫(SO2);二氧化氮(NO2);可吸入颗粒物(PM2.5).
故答案为:空气污染指数(API);二氧化硫(SO2);二氧化氮(NO2);可吸入颗粒物(PM2.5).
点评:本题考查环境污染知识,为高频考点,侧重于化学与生活、环境的考查,有利于培养学生良好的科学素养,树立保护环境的意识,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
下列各组物质的稀溶液相互反应,把前者逐滴滴入后者与把后者逐滴滴入前者,所产生的现象不相同的是( )
| A、AlCl3和NaOH |
| B、NaOH和HCl |
| C、NaHCO3和HCl |
| D、NaCl和AgNO3 |
将下列各组物质区别开来的实验方案(见括号内的方法)不妥的是( )
| A、丝绸与棉布(采用灼烧闻其气味的方法) |
| B、Na2SO4与NH4Cl(采用加碱加热闻其气味的方法) |
| C、NaCl与KCl(采用灼烧时观察焰色的方法) |
| D、K2CO3与K2SO4(采用加BaCl2观察有无沉淀产生的方法) |
相同温度下,甲(恒容)、乙(恒压)、丙(恒容)3个密闭容器中发生可逆反应:2SO2(g)+O2(g)?2SO3(g)△H=-197kJ/mol.实验测得起始、平衡时的有关数据如下表.下列正确的是( )
| 容器 | 起始各物质的物质的量/mol | 达到平衡时体系能量的变化 | ||
| SO2 | O2 | Ar | ||
| 甲 | 2 | 1 | 0 | 放出热量:Q1 |
| 乙 | 2 | 1 | 0 | 放出热量:Q2 |
| 丙 | 2 | 1 | 0.5 | 放出热量:Q3 |
| A、Q1=Q3<Q2 |
| B、达到平衡时,乙容器中SO2的体积分数最大 |
| C、平衡时,甲、乙、丙3个容器中甲的平衡常数最小 |
| D、若在上述条件下,反应生成1mol SO3(s),则反应放热为98.5kJ |
用Pt做电极,电解含C(Cu2+):C(Na+):C(Cl-)=1:2:4的混合溶液,在任何情况下,阴、阳两极下不可能同时发生的反应是( )
| A、阴极:2H++2e-=H2↑ 阳极:4OH--4e-=2H2O+O2↑ |
| B、阴极:2H++2e-=H2↑ 阳极:2Cl--2e-=Cl2↑ |
| C、阴极:Cu2++2e-=Cu 阳极:4OH--4e-=2H2O+O2↑ |
| D、阴极:Cu2++2e-=Cu 阳极:2Cl--2e-=Cl2↑ |
一定温度和压强下N2+3H2?2NH3反应达到平衡后,下列说法中正确的是( )
| A、N2与H2不再化合,NH3不再分解 |
| B、N2、H2化合成氨的反应速率等于NH3 分解的反应速率 |
| C、H2、NH3的体积分数相等 |
| D、N2、H2、NH3的物质的量浓度相等 |
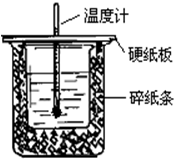 用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
用50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: