题目内容
4.某温度下,在恒容密闭容器中充入1molN2和3molH2,发生可逆反应:N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1达到平衡时,反应放出36.8kJ热量,则平衡时NH3的物质的量为( )| A. | 0.4mol | B. | 0.6mol | C. | 0.8mol | D. | 2mol |
分析 热化学方程式中为完全转化时的能量变化,物质的量与热量成正比,以此来解答.
解答 解:由N2(g)+3H2(g)?2NH3(g)△H=-92.4kJ•mol-1可知,生成2molNH3时放出的热量为92.4kJ,
达到平衡时,反应放出36.8kJ热量,则平衡时NH3的物质的量为$\frac{36.8kJ}{92.4kJ}$×2=0.8mol,
故选C.
点评 本题考查化学平衡的计算,为高频考点,把握热化学方程式的意义、物质的量与热量的关系为解答本题的关键,侧重分析与计算的考查,注意氨气的物质的量与热量成正比,题目难度不大.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
1.下列有关说法正确的是( )
| A. | 用pH试纸测得NaC1O溶液的pH为10 | |
| B. | 用澄清石灰水鉴别Na2CO3溶液与NaHCO3溶液 | |
| C. | 向Fe(NO3)2溶液中滴加稀盐酸,无明显现象 | |
| D. | 向K2Cr2O7溶液中滴加NaOH溶液,溶液逐渐变黄 |
2. J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期及中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等:M 是地壳中含虽最多的金属元素.请用化学用语填空..
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期及中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等:M 是地壳中含虽最多的金属元素.请用化学用语填空..
(1)元素T在周期表中的位置是第三周期、第ⅦA族.
(2)J和氢组成的化合物分子有6个原子,其电子式为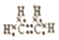 .
.
(3)写出工业冶炼M的化学方程式2Al2O3$\frac{\underline{\;\;\;通电\;\;\;}}{冰晶石}$4Al+3O2↑.
M和R形成的化合物在潮湿的空气中迅速变质,反应的化学方程式为Al2S3+6H2O=2Al(OH)3+3H2S↑.
(4)L的简单单气态氢化物甲的水溶液显碱性.
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2的淸除剂,所发生反应的产物不污染环境,其化学方程式为2NH3•H2O+3H2O2=N2↑+8H2O(或2NH3+3H2O2=N2↑+6H2O).
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,.仅改变下表中反应条件M,该平衡体系中随M递增N递减的是AC(选填序号).
③甲和O2组成的混合气共amol导入密闭反应器中,在催化剂存在下发生化学反应.若混合气体中O2为xmol.反应生成的HLO3为ymol.请填表和画出相应的函数图象.
 J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期及中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等:M 是地壳中含虽最多的金属元素.请用化学用语填空..
J、L、M、R、T是原子序数依次增大的短周期主族元素,J、R在周期及中的相对位置如下表;J元素最低负化合价的绝对值与其原子最外层电子数相等:M 是地壳中含虽最多的金属元素.请用化学用语填空..| J | ||||
| R |
(2)J和氢组成的化合物分子有6个原子,其电子式为
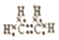 .
.(3)写出工业冶炼M的化学方程式2Al2O3$\frac{\underline{\;\;\;通电\;\;\;}}{冰晶石}$4Al+3O2↑.
M和R形成的化合物在潮湿的空气中迅速变质,反应的化学方程式为Al2S3+6H2O=2Al(OH)3+3H2S↑.
(4)L的简单单气态氢化物甲的水溶液显碱性.
①在微电子工业中,甲的水溶液可作刻蚀剂H2O2的淸除剂,所发生反应的产物不污染环境,其化学方程式为2NH3•H2O+3H2O2=N2↑+8H2O(或2NH3+3H2O2=N2↑+6H2O).
②一定条件下,甲在固定体积的密闭容器中发生分解反应(△H>0)并达平衡后,.仅改变下表中反应条件M,该平衡体系中随M递增N递减的是AC(选填序号).
| 选项 | A | B | C | D |
| M | 温度 | 温度 | H2的物质的量 | 甲的物质的量 |
| N | 甲的物质的量 | 平衡常数K | 甲的转化率 | 生成物总物质的量 |
| 甲转化为HLO3的情况 | X取值范围 | N(HLO3)y/mol |
| 无HLO3的生成 | y=0 | |
| 有部分HLO3的生成 | ||
| 全部生成HLO3 |
19.下列有关实验装置,能达到实验目的是( )

| A. | 用图1所示装置制取少量Cl2 | B. | 用图2所示装置制取干燥的NH3 | ||
| C. | 用图3制备并检验H2的可燃性 | D. | 用图4装置鉴别碳酸钠和碳酸氢钠 |
16.25℃时,三种酸的电离平衡常数如表:
回答下列问题:
(1)一般情况下,当温度升高时,Ka增大(填“增大”、“减小”或“不变”).
(2)下列反应不能发生的是cd(填序号)
a.CO32-+CH3COOH=CH3COO-+CO2↑+H2O b.ClO-+CH3COOH=CH3COO-+HClO
c.CO32-+2HClO=CO2↑+H2O+2ClO-d.2ClO-+CO2+H2O=CO32-+2HClO
(3)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验.资料:AgSCN是白色沉淀,相同温度下,溶解度:AgSCN>AgI.
1写出步骤2中溶液变红色的离子方程式Fe3++3SCN-?Fe(SCN)3
2步骤3中现象a是出现白色沉淀
3用化学平衡原理解释步骤4的实验现象AgSCN(s)?Ag+(aq)+SCN-(aq),加入KI后,因为溶解度:AgI<AgSCN,Ag+与I-反应生成AgI黄色沉淀:Ag++I-═AgI↓,AgSCN的溶解平衡正向移动.
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 |
(1)一般情况下,当温度升高时,Ka增大(填“增大”、“减小”或“不变”).
(2)下列反应不能发生的是cd(填序号)
a.CO32-+CH3COOH=CH3COO-+CO2↑+H2O b.ClO-+CH3COOH=CH3COO-+HClO
c.CO32-+2HClO=CO2↑+H2O+2ClO-d.2ClO-+CO2+H2O=CO32-+2HClO
(3)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验.资料:AgSCN是白色沉淀,相同温度下,溶解度:AgSCN>AgI.
| 操作步骤 | 现象 |
| 步骤1:向2mL 0.005mol•L-1 AgNO3溶液中加入2mL 0.005mol•L-1KSCN溶液,静置. | 出现白色沉淀. |
| 步骤2:取1mL上层清液于试管中,滴加1滴2mol•L-1 Fe(NO3)3溶液. | 溶液变红色. |
| 步骤3:向步骤2的溶液中,继续加入5滴3mol•L-1AgNO3溶液. | 出现白色沉淀,溶液红色变浅. |
| 步骤4:向步骤1余下的浊液中加入5滴3mol•L-1KI溶液. | 出现黄色沉淀. |
2步骤3中现象a是出现白色沉淀
3用化学平衡原理解释步骤4的实验现象AgSCN(s)?Ag+(aq)+SCN-(aq),加入KI后,因为溶解度:AgI<AgSCN,Ag+与I-反应生成AgI黄色沉淀:Ag++I-═AgI↓,AgSCN的溶解平衡正向移动.
14.下列说法中,正确的是( )
| A. | 乙醇和乙醚互为同分异构体 | |
| B. | 乙醇和乙二醇互为同系物 | |
| C. | 含羟基的化合物一定属于醇类 | |
| D. | 等质量的乙醇、乙二醇与足量钠反应时,乙二醇产生的氢气的量较乙醇的多 |
 短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.请回答下列问题:
短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.请回答下列问题: .
.
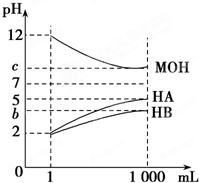 某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验:将pH=2的两种酸溶液HA、HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题:
某化学学习小组为研究HA、HB和MOH的酸碱性的相对强弱,设计以下实验:将pH=2的两种酸溶液HA、HB和pH=12的MOH碱溶液各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图,根据所给的数据,请回答下列问题: