题目内容
16.25℃时,三种酸的电离平衡常数如表:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10-5 | K1 4.3×10-7 K2 5.6×10-11 | 3.0×10-8 |
(1)一般情况下,当温度升高时,Ka增大(填“增大”、“减小”或“不变”).
(2)下列反应不能发生的是cd(填序号)
a.CO32-+CH3COOH=CH3COO-+CO2↑+H2O b.ClO-+CH3COOH=CH3COO-+HClO
c.CO32-+2HClO=CO2↑+H2O+2ClO-d.2ClO-+CO2+H2O=CO32-+2HClO
(3)为了研究沉淀溶解平衡和沉淀转化,某同学查阅资料并设计如下实验.资料:AgSCN是白色沉淀,相同温度下,溶解度:AgSCN>AgI.
| 操作步骤 | 现象 |
| 步骤1:向2mL 0.005mol•L-1 AgNO3溶液中加入2mL 0.005mol•L-1KSCN溶液,静置. | 出现白色沉淀. |
| 步骤2:取1mL上层清液于试管中,滴加1滴2mol•L-1 Fe(NO3)3溶液. | 溶液变红色. |
| 步骤3:向步骤2的溶液中,继续加入5滴3mol•L-1AgNO3溶液. | 出现白色沉淀,溶液红色变浅. |
| 步骤4:向步骤1余下的浊液中加入5滴3mol•L-1KI溶液. | 出现黄色沉淀. |
2步骤3中现象a是出现白色沉淀
3用化学平衡原理解释步骤4的实验现象AgSCN(s)?Ag+(aq)+SCN-(aq),加入KI后,因为溶解度:AgI<AgSCN,Ag+与I-反应生成AgI黄色沉淀:Ag++I-═AgI↓,AgSCN的溶解平衡正向移动.
分析 (1)弱电解质的电离为吸热过程;
(2)酸性强弱为CH3COOH>H2CO3>HClO>HCO3-,强酸能够制取弱酸,据此对各选项进行判断;
(3)①铁离子遇到硫氰化钾因发生反应而显示红色;
②银离子会和硫氰酸根离子之间反应得到AgSCN白色沉淀;
③沉淀向着更难溶的方向转化.
解答 解:(1)弱电解质的电离为吸热过程,升高温度促进电离,电离常数增大;
故答案为:增大;
(2)a.CO32-+CH3COOH═CH3COO-+CO2↑+H2O:碳酸的酸性小于CH3COOH,所以CH3COOH能够制取碳酸,该反应能够发生,故a不选;
b.ClO-+CH3COOH═CH3COO-+HClO:CH3COOH的酸性大于HClO,CH3COOH能够制取HClO,该反应能够发生,故b不选;
c.CO32-+HClO═CO2↑+H2O+ClO-:HClO的酸性小于碳酸,该反应无法发生,故c选;
d.2ClO-+CO2+H2O═CO32-+2HClO:由于酸性H2CO3>HClO>HCO3-,则碳酸与次氯酸根离子反应只能生成碳酸氢根离子,不会生成CO32-,该反应不能发生,故d选;
故答案为:cd;
(3)①铁离子遇到硫氰化钾显示红色,发生的反应为:Fe3++3SCN-?Fe(SCN)3,
故答案为:Fe3++3SCN-?Fe(SCN)3;
②加入硝酸银,银离子会和硫氰酸根离子之间反应得到AgSCN白色沉淀,
故答案为:出现白色沉淀;
③AgSCN(s)?Ag+(aq)+SCN-(aq),加入KI后,因为溶解度:AgI<AgSCN,沉淀会向着更难溶的方向转化,即Ag+与I-反应生成AgI黄色沉淀:Ag++I-═AgI↓,AgSCN的溶解平衡正向移动,
故答案为:AgSCN(s)?Ag+(aq)+SCN-(aq),加入KI后,因为溶解度:AgI<AgSCN,Ag+与I-反应生成AgI黄色沉淀:Ag++I-═AgI↓,AgSCN的溶解平衡正向移动.
点评 本题考查了弱电解质的电离、电离常数的应用、沉淀转化等,题目难度中等,试题知识点较多、综合性较强,充分考查学生分析判断能力及化学思维能力.

( )
| A. | KSCN溶液 | B. | BaCl2溶液 | C. | NaOH溶液 | D. | HCl溶液 |
| A. | FeCl3易溶于水,可用作净水剂 | |
| B. | 硅是半导体材料,纯净的硅是光纤制品的基本原料 | |
| C. | 浓硫酸能干燥氯气,说明浓硫酸具有吸水性 | |
| D. | 氨易液化,液氨气化吸收大量的热,所以液氨常用作制冷剂 |
| A. | 0.4mol | B. | 0.6mol | C. | 0.8mol | D. | 2mol |
| A. | CuFeS2中硫的化合价为-1价 | |
| B. | Fe2O3为氧化产物,SO2是还原产物 | |
| C. | lmolCuFeS2反应转移电子为13mol | |
| D. | 该反应的所有产物均既是氧化产物,又是还原产物 |
| A. | 小苏打溶液中:c(Na+)+c(H+)=c(HCO3-)+c(CO32-)+c(OH-) | |
| B. | CH3COONa溶液中:c(CH3COO-)>c(Na+) | |
| C. | 物质的量浓度相等的CH3COOH溶液和CH3COONa溶液等体积混合:c(CH3COO-)+2c(OH-)=2c(H+)+c(CH3COOH) | |
| D. | 常温下,0.1mol/L的NaHA溶液,其pH=4,则c(HA-)>c(H+)>c(H2A)>c(A2-) |
| A. | Au-e-═Au+ | B. | O2+2H2O+4e-═4OH- | ||
| C. | Au-e-+2CN-═Au(CN)2- | D. | 2H2O+2e-═2OH-+H2 |
| A. | 无法判断该溶液中是否含有K+ | |
| B. | 该溶液中一定含有K+、SiO32-,可能含有CO32- | |
| C. | 该溶液中无SO32-,一定含有CO32- | |
| D. | 该溶液中可能含有K+和CO32- |
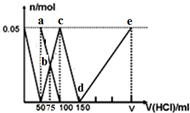
| A. | a点溶液中:c(HCO3-)+2c(H2CO3)+c(H+)=c(OH-) | |
| B. | b点所得溶液中有:c(Na+)>c(Cl-)>c(HCO3-)=c(CO32-)>c(OH-) | |
| C. | c点溶液中:c(Cl-)+c(HCO3-)+c(H2CO3)+c(CO32-)=0.75 mol/L | |
| D. | 原混合溶液中:n(CO32-):n(AlO2-)=1:2 |