题目内容
5.在一个密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8mol•L-1和5.4mol•L-1,在一定的条件下发生反应N2(g)+3H2(g)?2NH3(g).10min后测得N2的浓度是0.8mol•L-1,则在这10min内NH3的平均反应速率是( )| A. | 0.1mol•L-1•min-1 | B. | 0.6mol•L-1•min-1 | ||
| C. | 0.3mol•L-1•min-1 | D. | 0.2mol•L-1•min-1 |
分析 10min内 v(N2)=$\frac{△c}{△t}$=$\frac{(1.8-0.8)mol/L}{10min}$=0.1mol/(L.min),同一可逆反应同一时间段内,各物质的反应速率之比等于其计量数之比,据此计算氨气的反应速率.
解答 解:10min内 v(N2)=$\frac{△c}{△t}$=$\frac{(1.8-0.8)mol/L}{10min}$=0.1mol/(L.min),同一可逆反应同一时间段内,各物质的反应速率之比等于其计量数之比,则v(NH3)=2 v(N2)=2×0.1mol/(L.min)=0.2mol/(L.min),故选D.
点评 本题考查化学反应速率的有关计算,侧重考查分析计算能力,明确反应速率与计量数关系即可解答,注意单位之间的换算,题目难度不大.

练习册系列答案
相关题目
15.复合材料制成的防弹头盔能抵御多种手枪子弹的射击,最大限度地保护使用人员的安全,下列有关复合材料的性质中,与这一用途有关的是( )
| A. | 高强度、质量轻 | B. | 耐热、抗高温 | C. | 耐腐蚀、稳定性好 | D. | 导电、导热性好 |
13.下列说法错误的是( )
| A. | NH4+和CH4属于等电子体,立体构型都是正四面体 | |
| B. | 主族元素的原子核外电子最后填入的能级是s能级或p能级 | |
| C. | BF3、NCl3、H2O分子中所有原子都满足最外层为8电子结构的是NCl3 | |
| D. | 向盛有硫酸铜溶液的试管里加入过量氨水,将得到蓝色的氢氧化铜沉淀 |
20.化学式为C8H16O2的有机物A在酸性条件下能水解生成C和D,且C在一定条件下能转化为D,则有机物A的结构可能有( )
| A. | 1 种 | B. | 2 种 | C. | 3 种 | D. | 4 种 |
10.红葡萄酒密封时间越长,则香味越浓郁,其原因是久置的葡萄酒中,与原来相比含有更多的( )
| A. | (C6H10O5)n | B. | CH3CH2OH | C. | CH3COOH | D. | CH3COOC2H5 |
17.下列试剂:①浓氨水 ②氯水 ③硝酸银 ④浓硝酸 ⑤浓盐酸 ⑥溴化银,其中必须用棕色试剂瓶盛装的有( )
| A. | ①②③④⑤⑥ | B. | ②③④⑥ | C. | ②③⑤⑥ | D. | ①③④⑤ |
14.某种兴奋剂的结构简式如图所示:有关该物质的说法正确的是( )


| A. | 遇FeCl3溶液呈紫色,且该物质与苯酚属于同系物 | |
| B. | 滴入酸性KMnO4溶液振荡,紫色褪去,能证明其结构中存在碳碳双键 | |
| C. | 1mol该物质分别与浓溴水和H2反应时最多消耗Br2和H2的物质的量分别为6mol和7mol | |
| D. | 该分子中的所有碳原子可能共平面 |
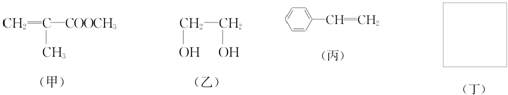
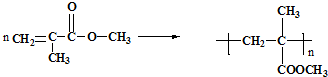
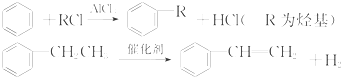 利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是
利用上述信息,以苯、乙烯、氯化氢为原料经三步反应合成丙,其中属于取代反应的化学方程式是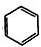 +CH3CH2Cl$→_{△}^{AlCl_{3}}$
+CH3CH2Cl$→_{△}^{AlCl_{3}}$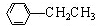 +HCl.
+HCl. 氢氧燃料电池是符合绿色化学理念的新型发电装置.如图所示为电池示意图,该电池电极表面均匀地镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.
氢氧燃料电池是符合绿色化学理念的新型发电装置.如图所示为电池示意图,该电池电极表面均匀地镀一层细小的铂粉,铂吸附气体的能力强,性质稳定.