��Ŀ����
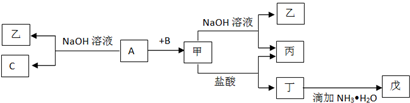
��֪AΪ��ѧ��ѧ�еij���������X��YΪ�����ǽ�����X��E��F��G��J������Ϊ���壬CΪ��ɫҺ�壬B��һ���Σ������ֽ⣮����A��ʯī���缫��B��Ũ��Һ������ʣ�����ԭ��أ��й�����֮���ת����ϵ��ͼ�����ַ�Ӧ�������������ﱻ��ȥ����

����д���пհף�
��1������AΪ ������a�ǽ�D��Һ��HCl���������ɣ�ԭ����
��2����Ӧ�ڵĻ�ѧ����Ϊ�� ����Ӧ�ݵĻ�ѧ���̣� ��
��3��ԭ��ط�Ӧ���У�������ӦʽΪ�� ��

����д���пհף�
��1������AΪ
��2����Ӧ�ڵĻ�ѧ����Ϊ��
��3��ԭ��ط�Ӧ���У�������ӦʽΪ��
���㣺������ƶ�
ר�⣺�ƶ���
�����������ͻ�ƿ���������һ��CΪ��ɫҺ�壬������X��X��ԭ��ط�Ӧ�õ���������H2����������Ӧ�õ�����CӦ��H2O��X��H2�����ݷ�Ӧ�߿�֪Y�Ƿǽ���C������E��F��G��H�����ڳ���������E�����������õ�����G������ѧ�ο��Ƴ�EΪNH3��FΪNO��GΪNO2����HΪHNO3�����ɷ�Ӧ�ݿ�֪J��CO2���ɷ�Ӧ�ܽ�һ���Ƴ�AΪMg����DΪMgCl2����Ϸ�Ӧ�ٿ���֪BΪNH4Cl���ݴ˽��
���
�⣺�����ͻ�ƿ���������һ��CΪ��ɫҺ�壬������X��X��ԭ��ط�Ӧ�õ���������H2����������Ӧ�õ�����CӦ��H2O��X��H2�����ݷ�Ӧ�߿�֪Y�Ƿǽ���C������E��F��G��H�����ڳ���������E�����������õ�����G������ѧ�ο��Ƴ�EΪNH3��FΪNO��GΪNO2����HΪHNO3�����ɷ�Ӧ�ݿ�֪J��CO2���ɷ�Ӧ�ܽ�һ���Ƴ�AΪMg����DΪMgCl2����Ϸ�Ӧ�ٿ���֪BΪNH4Cl��
��1��������������֪������AΪþ��������Һ��Mg2++2H2O?Mg��OH��2+2H+���ʲ���a�ǽ�MgCl2��Һ��HCl���������ɣ���ֹ�������ӣ�Mg2+��ˮ�⣬
�ʴ�Ϊ��þ����ֹ�������ӣ�Mg2+��ˮ�⣻
��2����Ӧ���ǰ��Ĵ���������Ӧ��ѧ����Ϊ��4NH3+5O2
4NO+6H2O��
��Ӧ����̼��Ũ���ᷴӦ����CO2��NO2��H2O������ʽΪ��C+4HNO3��Ũ��
CO2��+4NO2��+2H2O��
�ʴ�Ϊ��4NH3+5O2
4NO+6H2O��C+4HNO3��Ũ��
CO2��+4NO2��+2H2O��
��3��ԭ��ط�Ӧ���У�����������ԭ��Ӧ��笠����ӷŵ����ɰ�����������������ӦʽΪ��2NH4++2e-=2NH3��+H2����
�ʴ�Ϊ��2NH4++2e-=2NH3��+H2����
��1��������������֪������AΪþ��������Һ��Mg2++2H2O?Mg��OH��2+2H+���ʲ���a�ǽ�MgCl2��Һ��HCl���������ɣ���ֹ�������ӣ�Mg2+��ˮ�⣬
�ʴ�Ϊ��þ����ֹ�������ӣ�Mg2+��ˮ�⣻
��2����Ӧ���ǰ��Ĵ���������Ӧ��ѧ����Ϊ��4NH3+5O2
| ||
| �� |
��Ӧ����̼��Ũ���ᷴӦ����CO2��NO2��H2O������ʽΪ��C+4HNO3��Ũ��
| ||
�ʴ�Ϊ��4NH3+5O2
| ||
| �� |
| ||
��3��ԭ��ط�Ӧ���У�����������ԭ��Ӧ��笠����ӷŵ����ɰ�����������������ӦʽΪ��2NH4++2e-=2NH3��+H2����
�ʴ�Ϊ��2NH4++2e-=2NH3��+H2����
���������⿼��������ƶϣ�������ѧ���ķ���������Ԫ�ػ�����֪ʶ���ۺ����õĿ��飬Ϊ�߿��������ͣ�ע����������Ϣ�����ת����ϵ�����ƶϣ���3��Ϊ�״��㣬��ԭ���ʵ��Ϊ笠�����ˮ�⣬Mg���������ӷ�Ӧ�����������Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
����������ë�����㷽���ǣ�������
| A����ϡ���� | B������������Һ |
| C�������ˮ | D���ڻ������� |
��һ��������[C3H5��OH��3]���ڼױ��У� �������Һ����Ԫ����������Ϊ��������
�������Һ����Ԫ����������Ϊ��������
 �������Һ����Ԫ����������Ϊ��������
�������Һ����Ԫ����������Ϊ��������| A�������� | B��8.7% |
| C��17.4% | D��4.35% |
�������ӷ���ʽ��д��ȷ���ǣ�������
| A��Fe2O3��������Fe2O3+6HI=2Fe3++6I-+3H2O |
| B��Na2S��Һ�Լ��ԣ�S2-+2H2O=H2S+2OH- |
| C��CH3COOH��NaOH��Һ��Ӧ��H++2OH-=H2O |
| D��AgNO3��Һ�м��������ˮ��Ag++2NH3?H2O=Ag��NH3��2++2H2O |
������������ȷ���ǣ�����NA���������ӵ�������ֵ����������
| A��0.1 mol13C18O������������Ϊ1.7NA |
| B����0.1molFeCl3��ȫˮ���Ƴɽ��壬���ý���������Ϊ0.1NA |
| C����⾫��ͭת��NA������ʱ����������32 gͭ |
| D����״���£�22.4 L Cl2ͨ��������ʯ�������Ʊ�Ư�ۣ�ת�Ƶĵ�����ΪNA |