题目内容
检验氯化氢气体中是否混有Cl2,可采用的方法是( )
| A、用干燥的蓝色石蕊试纸 |
| B、用干燥有色布条 |
| C、将气体通入AgNO3溶液 |
| D、用湿润的淀粉碘化钾试纸 |
考点:氯气的化学性质
专题:
分析:氯气遇湿润的淀粉碘化钾试纸使之变蓝,遇到湿润的有色布条使之褪色,以此来解答.
解答:
解:A、氯气遇到湿润的有色物质,Cl2+H2O=HClO+HCl,生成的HClO具有漂白性,但氯气不能用干燥的蓝色石蕊试纸检验,故A错误;
B、用干燥有色布条,氯气不能与水反应生成次氯酸,不能使之褪色,故B错误;
C、气体中通入硝酸银溶液中,氯化氢反应生成氯化银白色程沉淀,氯气通入也会和水反应生成氯化氢与硝酸银反应生成白色沉淀,故C错误;
D、气体遇湿润的淀粉碘化钾试纸,Cl2+2I-=I2+2Cl-,碘单质遇淀粉变蓝,可检验,故D正确;
故选D.
B、用干燥有色布条,氯气不能与水反应生成次氯酸,不能使之褪色,故B错误;
C、气体中通入硝酸银溶液中,氯化氢反应生成氯化银白色程沉淀,氯气通入也会和水反应生成氯化氢与硝酸银反应生成白色沉淀,故C错误;
D、气体遇湿润的淀粉碘化钾试纸,Cl2+2I-=I2+2Cl-,碘单质遇淀粉变蓝,可检验,故D正确;
故选D.
点评:本题考查氯气的性质,为高频考点,把握物质的性质、发生的反应及现象为解答的关键,侧重氯气检验的考查,注意二者性质的差异,题目难度不大.

练习册系列答案
相关题目
下列说法正确的是( )
| A、在晶体中只要有阳离子就一定有阴离子 |
| B、加热至沸腾蒸发水分时,溶液的浓度一定增大 |
| C、一个原子或单核离子,最外层有8个电子时,一定达到了稳定结构 |
| D、水的分子量不到空气平均分子量的2/3,如果水分子间没有特殊的作用力,地球上就不会有液态水 |
下列实验操作中正确的是( )
| A、进行蒸发操作时,应将混合物中的水分完全蒸干后,才能停止加热 |
| B、进行蒸馏操作时,蒸馏烧瓶中应加入几粒沸石 |
| C、进行分液操作时,分液漏斗中下层液体先从下口放出,上层液体后从下口放出 |
| D、进行萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
下列叙述不正确的是( )
| A、淀粉、油脂、蛋白质都能水解,且水解产物各不相同 |
| B、从煤的干馏产物中可以获得焦炉气、粗氨水、煤焦油、焦炭等重要的化工原料 |
| C、石油催化裂化的主要目的是提高芳香烃的产量 |
| D、核酸是一类含磷的生物高分子化合物 |
下列有关离子反应或离子方程式的叙述中,正确的是( )
| A、能使pH试纸显深红色的溶液中,Fe3+、Cl-、Ba2+、Br-能大量共存 | ||||
B、惰性电极电解氯化铝溶液:2Cl-+2H2O
| ||||
| C、镁与极稀硝酸反应生成硝酸铵的离子方程式为:4Mg+6H++NO3-=4Mg2++NH4++3H2O | ||||
| D、将10 mL 0.1 mol?L-1 KAl(SO4)2溶液和10 mL 0.2 mol?L-1Ba(OH)2溶液混合,得到的沉淀中Al(OH)3和BaSO4的物质的量之比为1:2 |
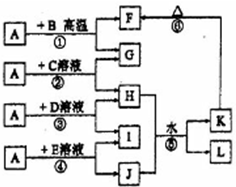 如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电导线材料,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答:
如图所示,A、G、I均为单质,其中A、G为金属且都常被用作输电导线材料,B为黑色粉末,L是由两种元素组成的盐,它是家庭厨房必备物品.请回答: