��Ŀ����
A��B��C��������ѧ��ѧ�����Ļ������ɫ��Ӧ���Ի�ɫ���ɷ�����ͼ��ʾ�仯������D��E��Ϊ��ɫ����ζ�����壮��Ӧ��������������ͼ��û�б����W��A��B�Ļ���

��1��A�Ļ�ѧʽΪ ��E�ĵ���ʽΪ ��
��2�������仯�У�����D�Ļ�ѧ��Ӧ����ʽΪ ��
��3��A��B�����ʵ���֮��Ϊm��n��ϼ��ȣ�
������ȫ��Ӧ�������C��D��H2O����m��n= ���÷�Ӧ�Ļ�ѧ����ʽΪ�� ��
������ȫ��Ӧ�������û��H2O����m��n= ��

��1��A�Ļ�ѧʽΪ
��2�������仯�У�����D�Ļ�ѧ��Ӧ����ʽΪ
��3��A��B�����ʵ���֮��Ϊm��n��ϼ��ȣ�
������ȫ��Ӧ�������C��D��H2O����m��n=
������ȫ��Ӧ�������û��H2O����m��n=
���㣺������ƶ�
ר�⣺�ƶ���
������A��B��C��������ѧ��ѧ�����Ļ������ɫ��Ӧ���Ի�ɫ��˵��ABC�к�����Ԫ�أ�����D��E��Ϊ��ɫ����ζ�����壬�����ͼ��ʾ�仯��Eͨ�����ʯ��ˮ���ɰ�ɫ������֤��EΪCO2��˵��AB�к���̼���Σ�W��ˮ��Ӧ����D��C��Һ��C��Һ����������̼��Ӧ����̼�����ƣ�AΪNaHCO3��CΪNa2CO3�����ж�BΪNa2O2���ݴ˷����жϽ���ش����⣻
���
�⣺A��B��C��������ѧ��ѧ�����Ļ������ɫ��Ӧ���Ի�ɫ��˵��ABC�к�����Ԫ�أ�����D��E��Ϊ��ɫ����ζ�����壬�����ͼ��ʾ�仯��Eͨ�����ʯ��ˮ���ɰ�ɫ������֤��EΪCO2��˵��AB�к���̼���Σ�W��ˮ��Ӧ����D��C��Һ��C��Һ����������̼��Ӧ����̼�����ƣ�AΪNaHCO3��CΪNa2CO3�����ж�BΪNa2O2����1��������������֪AΪNaHCO3��EΪCO2������ʽΪ�� ��
��
�ʴ�Ϊ��NaHCO3 �� ��
��
��2������D�Ļ�ѧ��Ӧ����ʽΪ�������ƺ�ˮ��Ӧ�����������ƺ���������������ƺ�ϡ���ᷴӦ���������ơ�ˮ����������Ӧ�Ļ�ѧ����ʽΪ��2Na2O2+2H2O�T4NaOH+O2�� �� 2Na2O2+2H2SO4�T2Na2SO4+O2��+2H2O��
�ʴ�Ϊ��2Na2O2+2H2O�T4NaOH+O2�� �� 2Na2O2+2H2SO4�T2Na2SO4+O2��+2H2O��
��3��A��B�����ʵ���֮��Ϊm��n��ϼ��ȷ�Ӧ��NaHCO3���ȷֽ�����̼���ơ�������̼��ˮ��������̼��ˮ��������Ʒ�Ӧ��
������ȫ��Ӧ�������CΪNa2CO3��DΪO2��H2O��˵�����ɵĶ�����̼�������Ʒ�Ӧ��2NaHCO3
Na2CO3+CO2��+H2O��2Na2O2+2CO2=Na2CO3+O2����m��n=4+2=2��1����Ӧ�Ļ�ѧ����ʽΪ��4NaHCO3+2Na2O2�T4Na2CO3+O2��+2H2O��
�ʴ�Ϊ��2��1��4NaHCO3+2Na2O2�T4Na2CO3+O2��+2H2O��
������ȫ��Ӧ�������û��H2O��˵��������̼��ˮȫ����������Ʒ�Ӧ��2NaHCO3
Na2CO3+CO2��+H2O��2Na2O2+2CO2=Na2CO3+O2��2Na2O2+2H2O=4NaOH+O2��
��ѧ����ʽ������ϵ��֪m��n=1��1��
�ʴ�Ϊ��1��1��
 ��
���ʴ�Ϊ��NaHCO3 ��
 ��
����2������D�Ļ�ѧ��Ӧ����ʽΪ�������ƺ�ˮ��Ӧ�����������ƺ���������������ƺ�ϡ���ᷴӦ���������ơ�ˮ����������Ӧ�Ļ�ѧ����ʽΪ��2Na2O2+2H2O�T4NaOH+O2�� �� 2Na2O2+2H2SO4�T2Na2SO4+O2��+2H2O��
�ʴ�Ϊ��2Na2O2+2H2O�T4NaOH+O2�� �� 2Na2O2+2H2SO4�T2Na2SO4+O2��+2H2O��
��3��A��B�����ʵ���֮��Ϊm��n��ϼ��ȷ�Ӧ��NaHCO3���ȷֽ�����̼���ơ�������̼��ˮ��������̼��ˮ��������Ʒ�Ӧ��
������ȫ��Ӧ�������CΪNa2CO3��DΪO2��H2O��˵�����ɵĶ�����̼�������Ʒ�Ӧ��2NaHCO3
| ||
�ʴ�Ϊ��2��1��4NaHCO3+2Na2O2�T4Na2CO3+O2��+2H2O��
������ȫ��Ӧ�������û��H2O��˵��������̼��ˮȫ����������Ʒ�Ӧ��2NaHCO3
| ||
��ѧ����ʽ������ϵ��֪m��n=1��1��
�ʴ�Ϊ��1��1��
���������⿼��������ת����ϵ�����жϣ��������ʺͷ�Ӧ����ķ���Ӧ�ã������������ʺͷ�Ӧ�����Ǽ���ؼ�����Ŀ�Ѷ��еȣ�

��ϰ��ϵ�д�
�����Ŀ
1.92gͭ��һ������Ũ���ᷴӦ������ͭ�IJ��ϼ��٣���Ӧ���ɵ�������ɫ��dz����Cuȫ����Ӧʱ�����ռ�����״��������1.12L����Ӧ������HNO3�����ʵ����ǣ�������
| A��0.12 mol |
| B��0.1 mol |
| C��0.11 mol |
| D��0.2 mol |
��������װ�úͲ������ܴﵽʵ��Ŀ���ǣ�������
A��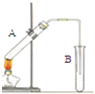 A��Ϊ�Ҵ������ᣬB��Ϊ����̼������Һ����ȡ�������� |
B��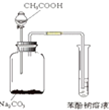 ��֤���ᡢ̼�ᡢ���ӵ�����ǿ�� |
C�� ��Ũ���ᡢ�Ҵ����ȵ�Լ170������ϩ |
D��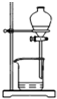 ��NaOH��Һ��ȥ���л��е��������� |
 B��
B��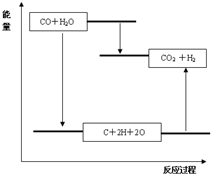
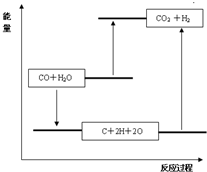 D��
D��