题目内容
13.北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).已知:C3H8(g)+5O2(g)→3CO2(g)+4H2O(l)△H=-2220.0kJ/mol
C3H6(g)+4.5O2(g)→3CO2(g)+3H2O(l)△H=-2049kJ/mol
下列说法正确的是( )
| A. | 1 mol C3H8(g)与5 mol O2(g)反应生成3 molCO2(g)和4 mol H2O(g)放出热量大于2220.0 kJ | |
| B. | 1 mol C3H6与4.5 mol O2反应生成3molCO2和3 mol H2O放出热量等于2049.0 kJ | |
| C. | 丙烷分子储存的能量大于丙烯分子 | |
| D. | 丙烷转化为丙烯的过程是一个吸热过程 |
分析 A、从液态水变为气态水是一个吸热的过程;
B、根据热化学方程式表示的意义来回答;
C、根据物质燃烧热的大小来比较;
D、根据反应物和产物能量的高低来判断反应的吸放热情况.
解答 解:A、根据态水变为气态水是一个吸热的过程,所以1molC3H8(g)与5molO2(g)反应生成3molCO2(g)和4molH2O(g)放出热量小于2220.0kJ,故A错误;
B、热化学方程式C3H6(g)+4.5O2(g)-→3CO2(g)+3H2O(l)+2049kJ表示的意义:在常温常压下,1molC3H6与4.5molO2反应生成3mol气体CO2和3mol液态H2O放出热量等于2049.0kJ,故B错误;
C、1mol丙烷完全燃烧放热多于1mol丙烯完全燃烧放热,所以丙烷分子储存的能量大于丙烯分子,故C正确;
D、丙烷分子储存的能量大于丙烯分子,所以丙烷转化为丙烯的过程是放热过程,故D错误.
故选C.
点评 本题考查学生热化学方程式的意义以及从物质具有的能量角度判断反应吸放热的方法,综合性强,难度不大.

练习册系列答案
相关题目
4.下列离子方程式中,不正确的是( )
| A. | KI的酸性溶液长期置于空气中:4I-+4H++O2═2I2+2H2O | |
| B. | 高锰酸钾酸性溶液与草酸溶液反应:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O | |
| C. | 用稀硫酸除去铁片表面的铁锈:Fe2O3+6H+═2Fe3++3H2O | |
| D. | 硫代硫酸钠溶液中滴加稀硫酸:2H++S2O32-═S↓+SO2↑+H2O |
1.已知下列热化学方程式:
C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1
现有0.2mol的炭粉和氢气组成的气、固混合物在氧气中完全燃烧,共放出63.53kJ热量,则炭粉与氢气的物质的量之比为( )
C(s)+O2(g)═CO2(g)△H=-393.5kJ•mol-1
2H2(g)+O2(g)═2H2O(g)△H=-483.6kJ•mol-1
现有0.2mol的炭粉和氢气组成的气、固混合物在氧气中完全燃烧,共放出63.53kJ热量,则炭粉与氢气的物质的量之比为( )
| A. | 1:1 | B. | 1:2 | C. | 2:3 | D. | 3:2 |
8.下列各组物质中一定属于同系物的是( )
| A. | C3H4和C4H6 | B. | C2H5Cl和C3H6Cl2 | ||
| C. | CH2=CH2和CH2=CH-CH=CH2 | D. | C3H8和C5H12 |
5. 早在40年前,科学大师Heilbronner经过理论研究预测,应当有可能合成“莫比乌斯”形状的芳香族(大环)轮烯分子,这一预测在2003年被德国化学家合成证实.[18]-轮烯是一种大环轮烯,其结构简式如图,有关它的说法正确的是( )
早在40年前,科学大师Heilbronner经过理论研究预测,应当有可能合成“莫比乌斯”形状的芳香族(大环)轮烯分子,这一预测在2003年被德国化学家合成证实.[18]-轮烯是一种大环轮烯,其结构简式如图,有关它的说法正确的是( )
 早在40年前,科学大师Heilbronner经过理论研究预测,应当有可能合成“莫比乌斯”形状的芳香族(大环)轮烯分子,这一预测在2003年被德国化学家合成证实.[18]-轮烯是一种大环轮烯,其结构简式如图,有关它的说法正确的是( )
早在40年前,科学大师Heilbronner经过理论研究预测,应当有可能合成“莫比乌斯”形状的芳香族(大环)轮烯分子,这一预测在2003年被德国化学家合成证实.[18]-轮烯是一种大环轮烯,其结构简式如图,有关它的说法正确的是( )| A. | [18]-轮烯分子中所有原子不可能处于同一平面 | |
| B. | 1mol-[18]轮烯最多可与9mol氢气发生加成反应生成环烷烃 | |
| C. | [18]-轮烯的分子式为:C18H12 | |
| D. | [18]-轮烯与乙烯互为同系物 |
2.下列有关物质的表达式正确的是( )
| A. | 乙烯分子的比例模型示意图: | B. | 乙醇的分子式:CH3CH2OH | ||
| C. | 2-甲基-2-丁烯的键线式: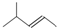 | D. | 硫化钠Na+[:$\underset{\stackrel{..}{S}}{..}$:]2Na+ |
3.经测定,由C3H7OH和C6H12组成的混合物中氢的质量分数为14%,则此混合物中碳的质量分数为( )
| A. | 78% | B. | 22% | C. | 14% | D. | 13% |

 ;B+G→F
;B+G→F +CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$
+CH3CH2OH$→_{△}^{浓H_{2}SO_{4}}$ .
.