题目内容
8.将5.000g的碳酸钠和碳酸氢钠的混合物进行加热,加热至质量不再减少时,混合物的质量减少了0.310g,则原混合物中碳酸钠的质量为( )| A. | 3.380g | B. | 4.580g | C. | 4.160g | D. | 4.410g |
分析 加热碳酸钠和碳酸氢钠的混合物,碳酸氢钠完全分解,根据反应的方程式2NaHCO3$\frac{\underline{\;加热\;}}{\;}$Na2CO3+CO2↑+H2O,利用差量法计算碳酸氢钠的质量,进而计算碳酸钠质量.
解答 解:碳酸钠较稳定,加热不分解,只有碳酸氢钠分解,
设混合物中含有NaHCO3的质量为x,则
2NaHCO3$\frac{\underline{\;加热\;}}{\;}$Na2CO3+CO2↑+H2O△m
2×84 62
x 0.31
$\frac{2×84}{x}=\frac{62}{0.31}$,解得:x=0.84g,
所以:m(Na2CO3)=5g-m(NaHCO3)=5g-0.84g=4.16g,
故选:C.
点评 本题考查混合物的计算,难度不大,注意碳酸氢钠的性质,利用差量法计算简化计算过程.

练习册系列答案
 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案
相关题目
18.下列对有机物结构或性质的描述中,错误的是( )
| A. | 乙醇通过消去反应可制得乙烯 | |
| B. | CH3CH=CHCH3分子中的4个碳原子在同一平面上 | |
| C. | 乙烷和丙烯的物质的量共1mol,完全燃烧生成3molH2O | |
| D. | 在溴水中加入苯,振荡后溴水的颜色变浅,这是由于发生了加成反应 |
19.设NA为阿伏加德罗常数的数值,下列有关叙述正确的是( )
| A. | 100g 98%的浓硫酸中含有的氢原子数目为2NA | |
| B. | 16g16O2和18O2的混合物中含有的质子数目为8NA | |
| C. | 电解精炼铜的过程中,若阳极减重64g,则电路中一定通过2NA个电子 | |
| D. | 取50ml14.0mol/L浓硝酸与足量的铜片反应,生成气体分子的数目可能为0.25NA |
16.下列变化需要克服共价键的是( )
| A. | 干冰的升华 | B. | 硅的熔化 | C. | 氯化钾的溶解 | D. | 汞的气化 |
3.下列分子中,属干含有极性健的非极性分子的是( )
| A. | H2O | B. | Br2 | C. | CH4 | D. | HCl |
13.将后者逐渐滴入(或通入)前者至过量,有沉淀产生且最终消失的是( )
| A. | 氯化铝、氨水 | B. | 氢硫酸、氧气 | C. | 硫酸铝、氢氧化钠 | D. | 氯化亚铁、氯气 |
20.小苏打是常用的食品添加剂,其化学式是( )
| A. | Na2CO3 | B. | NaHCO3 | C. | Na2SO4 | D. | NaCl |
10.化学反应A2+B2=2AB的能量变化如图,则下列正确的是( )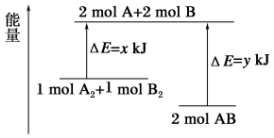

| A. | 该反应是吸热反应 | |
| B. | 断裂1molA-A键和1molB-B键可放出X kJ的能量 | |
| C. | 2molAB的总能量高于1molA2和1molB2的总能量 | |
| D. | 断裂2molA-B键需吸收YKJ的能量 |