题目内容
向醋酸溶液中加入醋酸钠,使溶液的pH=7,下列对这一溶液的说法正确的是( )
| A、溶液中醋酸的浓度与醋酸钠的浓度恰好相等 |
| B、溶液中醋酸根离子浓度小于钠离子浓度 |
| C、此时醋酸的电离程度与醋酸钠的水解程度相等 |
| D、该溶液中醋酸没有电离,醋酸钠也没有水解 |
考点:弱电解质在水溶液中的电离平衡
专题:电离平衡与溶液的pH专题
分析:醋酸钠是强碱弱酸盐,醋酸根离子水解导致醋酸钠溶液呈弱碱性,加入醋酸使其混合溶液呈中性,则应该加入少量醋酸即可,所以醋酸浓度远远小于醋酸钠浓度,混合溶液呈醋酸电离程度等于醋酸根离子水解程度.
解答:
解:A.醋酸钠溶液呈弱碱性,加入醋酸使混合溶液呈中性,则加入极少量醋酸即可,所以醋酸钠浓度远远大于醋酸浓度,故A错误;
B.溶液呈中性,则c(H+)=c(OH-),根据电荷守恒得C(CH3COO-)=c(Na+),故B错误;
C.混合溶液中醋酸电离程度等于醋酸根离子水解程度,导致溶液中c(H+)=c(OH-),溶液呈中性,故C正确;
D.该溶液中醋酸电离、醋酸根离子水解,但醋酸电离程度等于醋酸根离子水解程度,所以溶液呈中性,故D错误;
故选C.
B.溶液呈中性,则c(H+)=c(OH-),根据电荷守恒得C(CH3COO-)=c(Na+),故B错误;
C.混合溶液中醋酸电离程度等于醋酸根离子水解程度,导致溶液中c(H+)=c(OH-),溶液呈中性,故C正确;
D.该溶液中醋酸电离、醋酸根离子水解,但醋酸电离程度等于醋酸根离子水解程度,所以溶液呈中性,故D错误;
故选C.
点评:本题考查了弱电解质的电离及盐类水解,根据其电离程度和水解程度相对大小确定溶液酸碱性,再结合电荷守恒分析解答,题目难度不大.

练习册系列答案
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
相关题目
下列反应属于氧化还原反应的是( )
| A、H2SO4+2NaOH═Na2SO4+2H2O | ||||
B、MnO2+4HCl
| ||||
| C、NH3+HCl═NH4Cl | ||||
D、2NaHCO3
|
下列强电解质、弱电解质、非电解质的分类,正确的一组是( )
| A | B | C | D | |
| 强电解质 | CH3COOH | NaOH | BaSO4 | CuSO4 |
| 弱电解质 | Al | CH3COOH | CaCO3 | NH3?H2O |
| 非电解质 | CO2 | 金刚石 | 水银 | 酒精 |
| A、A | B、B | C、B | D、D |
有一种高分子材料称为“塑料王”,它的成分是( )
| A、聚乙烯 | B、聚苯乙烯 |
| C、聚四氟乙烯 | D、聚氨酯树脂 |
在一定温度下发生可逆反应A(g)+3B(g)?2C(g),下列叙述中,不能判断该反应达到平衡的是
(1)C生成速率与C分解速率相等.
(2)单位时间内生成amolA,同时生成3amolB
(3)A、B、C的浓度不再变化.
(4)单位时间内消耗amolA,同时生成3amolB
(5)A、B、C的分子数之比为1:3:2.
(6)混合气体的物质的量不再变化.( )
(1)C生成速率与C分解速率相等.
(2)单位时间内生成amolA,同时生成3amolB
(3)A、B、C的浓度不再变化.
(4)单位时间内消耗amolA,同时生成3amolB
(5)A、B、C的分子数之比为1:3:2.
(6)混合气体的物质的量不再变化.( )
| A、(2)(5) |
| B、(1)(4)(6) |
| C、(2)(4) |
| D、(3)(4) |
在NH4Cl溶液中,下列关系正确的是( )
| A、c (Cl-)>c (NH4+)>c (H+)>c (OH-) |
| B、c (NH4+)>c (Cl-)>c (H+)>c (OH-) |
| C、c (NH4+)=c (Cl-)>c (H+)=c (OH-) |
| D、c (Cl-)=c (NH4+)>c (H+)>c (OH-) |
今有pH相同的硫酸和醋酸各100mL,将足量的镁条分别加入到硫酸溶液和醋酸溶液中,关于反应的叙述正确的是( )
| A、因为硫酸是强电解质,在水溶液中完全电离,所以刚开始其反应速率更快 |
| B、整个反应过程中两者的反应速率相同 |
| C、镁与硫酸反应产生的氢气比醋酸与镁反应产生的氢气少 |
| D、硫酸的物质的量浓度大于醋酸 |
下列化合物中,含有非极性键的离子化合物是( )
①Ba(OH)2 ②H2SO4 ③Na2O2 ④CaCl2.
①Ba(OH)2 ②H2SO4 ③Na2O2 ④CaCl2.
| A、③ | B、①③④ |
| C、③④ | D、①②③④ |
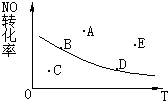 2NO+O2?2NO2+Q,NO的最大转化率与温度的关系图上标有A、B、C、D、E五点,其中表示未达到平衡状态且υ正>υ逆的是( )
2NO+O2?2NO2+Q,NO的最大转化率与温度的关系图上标有A、B、C、D、E五点,其中表示未达到平衡状态且υ正>υ逆的是( )