题目内容
9.为测定某有机化合物A的结构,进行如下实验.[分子式的确定]
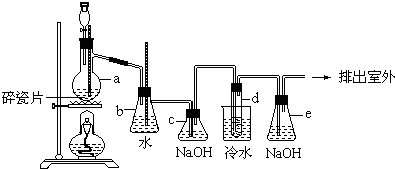
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4g H2O和8.8g CO2,消耗氧气6,.72L(标准状况下),则该物质中各元素的原子个数比是2:6:1.
(2)质谱仪测定该有机化合物的相对分子质量为46,则该物质的分子式是C2H6O.
(3)根据价键理论,预测A的可能结构并写出其结构简式CH3CH2OH或CH3OCH3.
[结构式的确定]
(4)1H核磁共振谱能对有机物分子中不同位置的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目.例如:甲基氯甲基醚(Cl-CH2-O-CH3)有两种氢原子(如图1).经测定,有机物A的1H核磁共振谱示意图如图2所示,则A的结构简式为CH3CH2OH.

[性质实验]
(5)A在一定条件下脱水可生成B,B可合成塑料C,请写出B转化为C的化学方程式:

(6)体育比赛中当运动员肌肉扭伤时,队医随即用氯乙烷(沸点为12.27℃)对受伤部位进行局部冷冻麻醉.请用B选择合适的方法制备氯乙烷,要求原子利用率为100%,请写出制备反应的化学方程式:CH2=CH2+HCl$→_{△}^{催化剂}$CH3CH2Cl.
分析 (1)浓硫酸增重为水的质量,碱石灰增重为二氧化碳的质量,以此可确定有机物中C、H原子个数比值,结合消耗氧气的体积可确定有机物中各原子个数比值;
(2)根据有机物原子个数比值可确定最简式,结合相对分子质量可确定有机物分子式;
(3)根据有机物分子式结合价键理论可确定有机物的可能结构;
(4)有机物A分子中有三种不同化学环境的氢原子,应为乙醇,二甲醚只有一种不同化学环境的氢原子;
(5)乙醇在一定条件下脱水可生成B,B为CH2=CH2,B可合成包装塑料C,C为聚乙烯,写出乙烯生成聚乙烯的化学方程式;
(6)原子利用率为100%,可用乙烯与HCl加成方法制备氯乙烯.
解答 解:(1)n(C)=n(CO2)=$\frac{8.8g}{44g/mol}$=0.2mol,n(H)=2n(H2O)=$\frac{5.4g}{18g/mol}$×2=0.6mol,由题意可知n(H2O)=$\frac{5.4g}{18g/mol}$=0.3mol,n(CO2)=$\frac{8.8g}{44g/mol}$=0.2mol,n(O2)=$\frac{6.72L}{22.4L/mol}$=0.3mol,
根据氧原子守恒可知有机物中含有:n(O)=0.3mol+0.2mol×2-0.3mol×2=0.1mol,
则有机物中N(C):N(H):N(O)=0.2mol:0.6mol:0.1mol=2:6:1,
故答案为:2:6:1;
(2)该物质中各元素的原子个数比为N(C):N(H):N(O)=2:6:1,则最简式为C2H6O,其相对分子质量为46,则有机物的分子式为C2H6O,
故答案为:C2H6O;
(3)有机物的分子式为C2H6O,分子中可能存在C-C、C-H、C-O、O-H等化学键,可能的结构简式有CH3CH2OH或CH3OCH3,
故答案为:CH3CH2OH或CH3OCH3;
(4)有机物A分子中有三种不同化学环境的氢原子,应为乙醇,即CH3CH2OH,二甲醚只有一种不同化学环境的氢原子,
故答案为:CH3CH2OH;
(5)乙醇在一定条件下脱水可生成B,B为CH2=CH2,B可合成包装塑料C,C为聚乙烯,乙烯生成聚乙烯的化学方程式为 ,
,
故答案为: ;
;
(6)原子利用率为100%,可用乙烯与HCl加成方法制备,反应的方程式为:CH2=CH2+HCl$→_{△}^{催化剂}$CH3CH2Cl,故答案为:CH2=CH2+HCl$→_{△}^{催化剂}$CH3CH2Cl.
点评 本题考查有机物分子式、结构简式的确定,题目难度中等,本题注意从质量守恒的角度判断有机物最简式是解答该题的关键,试题培养了学生的分析能力及化学计算能力.

 暑假衔接教材期末暑假预习武汉出版社系列答案
暑假衔接教材期末暑假预习武汉出版社系列答案 假期作业暑假成长乐园新疆青少年出版社系列答案
假期作业暑假成长乐园新疆青少年出版社系列答案| A. | 0.1mol/L的盐酸和0.1mol/L的氢氧化钠溶液 | |
| B. | 0.1mol/L的盐酸和0.05mol/L的氢氧化钡溶液 | |
| C. | pH=3的醋酸和pH=11的氢氧化钠溶液 | |
| D. | pH=3的盐酸和pH=l1的氨水 |
| A. | 观察是否发生了化合反应 | |
| B. | 观察是否有氧气参加反应 | |
| C. | 观察是否有单质参加反应 | |
| D. | 观察反应前后是否有元素的化合价发生变化 |
| A. | 乙烯气体通入溴的四氯化碳溶液 | |
| B. | 加热浓硝酸和苯(浓硫酸作催化剂)制取硝基苯 | |
| C. | 加热溴乙烷和氢氧化钾的水溶液 | |
| D. | 加热溴乙烷和氢氧化钾的醇溶液 |