题目内容
24.5g H2SO4的物质的量是多少?1.50mol Na2CO3的质量是多少?
考点:物质的量的相关计算
专题:计算题
分析:根据n=
计算硫酸的物质的量;根据m=nM计算碳酸钠的质量.
| m |
| M |
解答:
解:硫酸的摩尔质量为98g/mol,24.5g H2SO4的物质的量是
=0.25mol;
碳酸钠的摩尔质量为106g/mol,1.50mol Na2CO3的质量是1.5mol×106g/mol=159g,
答:24.5g H2SO4的物质的量是0.25mol,1.50mol Na2CO3的质量是159g.
| 24.5g |
| 98g/mol |
碳酸钠的摩尔质量为106g/mol,1.50mol Na2CO3的质量是1.5mol×106g/mol=159g,
答:24.5g H2SO4的物质的量是0.25mol,1.50mol Na2CO3的质量是159g.
点评:本题考查物质的量有关计算,比较基础,注意掌握以物质的量为中心的有关计算公式.

练习册系列答案
相关题目
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9.单质Y和W都可与浓的NaOH溶液反应.下列说法不正确的是( )
| A、原子半径:Y>Z>W |
| B、非金属性最强的元素为W |
| C、Y的最高价氧化物对应的水化物不是强碱 |
| D、XW2分子中各原子最外层电子均达到电子结构 |
下列物质属于电解质的是( )
| A、Cu |
| B、CO2 |
| C、KNO3 |
| D、乙醇 |
晚自习的课间,同学们站在学校4楼上,可以看到在容桂街道的空中有移动的光柱,这就是气溶胶中发生的丁达尔现象,下列分散系不能发生丁达尔现象的( )
| A、豆浆 |
| B、Fe(OH)3胶体 |
| C、食盐水 |
| D、烟、云、雾 |
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
A、CO2的电子式 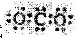 | ||
B、Cl-的结构示意图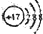 | ||
| C、H216O、D216O、H218O、D216O互为同素异形体 | ||
D、质量数为37的氯原子
|
下列离子方程式正确的是( )
| A、碳酸钙和盐酸反应 CO32-+2H+=H2O+CO2↑ |
| B、向氢氧化钡溶液中加硫酸溶液 Ba2++SO42-=BaSO4↓ |
| C、向稀盐酸溶液中加铁 3Fe十6H+=2Fe3++3H2↑ |
| D、向硝酸银溶液中加盐酸 Ag+十Cl-=AgCl↓ |
 原子序数依次增大的X、Y、Z、W是周期表中前30号元素,其中只有X、Y同周期.已知X的最外层电子数是其内层电子数的2倍;X与Y形成的常见化合物之一常被用于高炉炼铁;Z与X同主族,其单质在同周期元素中形成的单质中熔点最高;W原子核外的未成对电子数是前四周期元素中最多的.请回答下列问题:
原子序数依次增大的X、Y、Z、W是周期表中前30号元素,其中只有X、Y同周期.已知X的最外层电子数是其内层电子数的2倍;X与Y形成的常见化合物之一常被用于高炉炼铁;Z与X同主族,其单质在同周期元素中形成的单质中熔点最高;W原子核外的未成对电子数是前四周期元素中最多的.请回答下列问题: