题目内容
(1)氟里昂是freon的音译名,氟里昂的商业代号可用HFC-nmp表示,其中数字n等于碳原子数目减1(如果是0就省略),数字m等于氢原子数目加1,数字p等于氟原子数,氯原子数目不列.氟里昂CH2F-CHF2的代号为 ,它属于 (选填:A.一卤代烃 B.多卤代烃 C.饱和卤代烃 D.不饱和卤代烃 E:芳香卤代烃)类有机物,其同分异构体的结构简式为 .
(2)由于氟里昂无毒,化学性质又极其稳定,被大量用于制冷剂、灭火剂、发泡剂等.但大气中的氟里昂在平流层中受紫外线照射,会分解产生Cl原子,而Cl原子化学性质比较活泼:
O3
O2+O Cl+O3→ClO+O2 O+ClO→Cl+O2
上述反应的总反应为 其反应过程中,Cl原子起 作用.
(3)近几年市面上推出的冰箱新产品--无氟冰箱,主要是为了 (单选)
A.氟里昂价格高,为了经济
B.保护生态自然环境
C.保护人类生存环境
D.吸收和阻挡紫外线
(4)石油产品裂解所得裂解气的平均组成可表示为CnHm(m>2n),经测定某裂解气中各气体的体积分数分别为:甲烷-4%、乙烯-50%、丙烯-10%、其余为丁二烯和氢气(气体体积均在同温同压下测定).若得到50mol乙烯,x mol丁二烯和y mol氢气.
则x+y= ,n/m= (请用含x的式子表示).
(2)由于氟里昂无毒,化学性质又极其稳定,被大量用于制冷剂、灭火剂、发泡剂等.但大气中的氟里昂在平流层中受紫外线照射,会分解产生Cl原子,而Cl原子化学性质比较活泼:
O3
| 光 |
| 光 |
上述反应的总反应为
(3)近几年市面上推出的冰箱新产品--无氟冰箱,主要是为了
A.氟里昂价格高,为了经济
B.保护生态自然环境
C.保护人类生存环境
D.吸收和阻挡紫外线
(4)石油产品裂解所得裂解气的平均组成可表示为CnHm(m>2n),经测定某裂解气中各气体的体积分数分别为:甲烷-4%、乙烯-50%、丙烯-10%、其余为丁二烯和氢气(气体体积均在同温同压下测定).若得到50mol乙烯,x mol丁二烯和y mol氢气.
则x+y=
考点:氟氯代烷对环境的影响
专题:有机化合物的获得与应用
分析:(1)依据mnp所代表的意义以及氟利昂的化学式计算即可;
(2)由①Cl+O3→ClO+O2、②O3→O+O2、③ClO+O→Cl+O2,将方程式①+②+③得方程式:2O3→3O2;
(3)推出的冰箱新产品--无氟冰箱,可保护臭氧层;
(4)要得到50molC2H4,则会生成4molCH4、10molC3H6.设生成x mol丁二烯(C4H6)和y molH2,列方程式计算.
(2)由①Cl+O3→ClO+O2、②O3→O+O2、③ClO+O→Cl+O2,将方程式①+②+③得方程式:2O3→3O2;
(3)推出的冰箱新产品--无氟冰箱,可保护臭氧层;
(4)要得到50molC2H4,则会生成4molCH4、10molC3H6.设生成x mol丁二烯(C4H6)和y molH2,列方程式计算.
解答:
解:(1)氟里昂CH2F-CHF2的中含有2个C,3个H,3个F,即n=2-1=2,m=3+1=4,p=3,故其代号为:HFC-143,氟利昂属于多氯代烃,且元素之间均以单键结合,属于饱和氯代烃,氟利昂的通分异构体是F均在同一个C上,即同分异构体为:CH3-CF3,故答案为:HFC-143; BC;CH3-CF3;
(2)由①Cl+O3→ClO+O2、②O3→O+O2、③ClO+O→Cl+O2,将方程式①+②+③得方程式:2O3→3O2,在此过程中Cl未消耗,故是催化剂,故答案为:2O3=3O2; 催化;
(3)根据题目所给新信息,科学家发现氟里昂在紫外线的照射下能分解出氯原子破坏臭氧层,故寻找新型制冷剂、不使用含氟冰箱,寻找新型制冷剂等,是为了保护人类生存环境,故C正确,故选C;
(4)要得到50molC2H4,则会生成4molCH4、10molC3H6.设生成x mol丁二烯(C4H6)和y molH2,且需要催化裂解a mol的CnHm.
则根据碳原子守恒可知:an=4+30+100+4x=134+4x,n=
根据氢原子守恒可知:am=16+60+200+6x+2y=276+6x+2y,
根据题意:x+y=100-4-50-10=36,m=
,
=
,故答案为:36;
.
(2)由①Cl+O3→ClO+O2、②O3→O+O2、③ClO+O→Cl+O2,将方程式①+②+③得方程式:2O3→3O2,在此过程中Cl未消耗,故是催化剂,故答案为:2O3=3O2; 催化;
(3)根据题目所给新信息,科学家发现氟里昂在紫外线的照射下能分解出氯原子破坏臭氧层,故寻找新型制冷剂、不使用含氟冰箱,寻找新型制冷剂等,是为了保护人类生存环境,故C正确,故选C;
(4)要得到50molC2H4,则会生成4molCH4、10molC3H6.设生成x mol丁二烯(C4H6)和y molH2,且需要催化裂解a mol的CnHm.
则根据碳原子守恒可知:an=4+30+100+4x=134+4x,n=
| 134+4x |
| a |
根据氢原子守恒可知:am=16+60+200+6x+2y=276+6x+2y,
根据题意:x+y=100-4-50-10=36,m=
| 348+4x |
| a |
| n |
| m |
| 67+2x |
| 174+2x |
| 67+2x |
| 174+2x |
点评:本题主要考查有机物的性质以及计算,能利用原子守恒进行有机化学反应的计算,对学生能力的考查较高,题目难度中等.

练习册系列答案
 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
 2011年8月,多家媒体报道部分山西老陈醋是由醋精勾兑而成,醋精就是冰醋酸.专家介绍,只要是符合国家标准的勾兑醋,是可以放心食用的.下列关于醋酸的说法中正确的是( )
2011年8月,多家媒体报道部分山西老陈醋是由醋精勾兑而成,醋精就是冰醋酸.专家介绍,只要是符合国家标准的勾兑醋,是可以放心食用的.下列关于醋酸的说法中正确的是( )| A、0.01mol?L-1的醋酸溶液的pH=2 |
| B、向某温度下的醋酸溶液中通入HCl气体,醋酸的电离常数Ka会增大 |
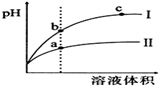
| C、等pH的盐酸与醋酸稀释后pH的变化如下图所示,则曲线I表示的是盐酸 |
| D、上图中,a、b、c三点表示的溶液的导电性强弱关系为b>a>c |
有关纤维素的说法,错误的是( )
| A、纤维素是一种天然高分子化合物 |
| B、纤维素是一种多糖,能够水解生成葡萄糖 |
| C、人体内含有能够促使纤维素水解的酶,纤维素在人体内能够被消化吸收 |
| D、纤维素是白色、没有气味和味道的纤维状结构的物质 |
2011年6月,云南省曲靖市发生了铬渣污染事件.在金属零件上镀铬后,既可以增加硬度,也可以有装饰的效果.如果在CrCl3溶液中,在铁制零件上镀铬,镀铬的阳极不用金属铬,而采用不溶性阳极.以下说法中正确的是( )
| A、铁制零件应该连接电源的负极 |
| B、阳极发生的电极反应为:Cr3++3e-=Cr |
| C、为了增强溶液的导电性,可以向溶液中加入一些溶于水的强电解质,提高溶液的pH |
| D、当通过1.5mol e-时,铁制零件上可沉积78g铬镀层 |
用惰性电极电解一定浓度的硫酸铜溶液,通电一段时间后,向所得的溶液中加入0.25molCu(OH)2固体后恰好恢复到电解前的浓度和pH.则电解过程中共转移电子的物质的量为( )
| A、0.25 mol |
| B、0.5 mol |
| C、0.75 mol |
| D、1.0mol |
下列各组离子在指定条件下能大量共存的是( )
| A、某无色溶液中:Na+,K+,MnO4-,SO42- |
| B、在pH=l的溶液中:Ca2+,Fe2+,Cl-,NO3- |
| C、含有HCO3-的溶液中:Na+,K+,Cl-,CO32- |
| D、在含大量的Fe3+溶液中:NH4+,Na+,Cl-,SCN- |

 (1)有下列几组物质,请将序号填入下列空格内:
(1)有下列几组物质,请将序号填入下列空格内: 和
和 